


Científicos obtienen una protección esterilizante en pruebas realizadas con una proteína recombinante de Plasmodium vivax. El estudio se realizó en ratones (imagen: Frontiers in Immunology)
Científicos obtienen una protección esterilizante en pruebas realizadas con una proteína recombinante de Plasmodium vivax. El estudio se realizó en ratones
Científicos obtienen una protección esterilizante en pruebas realizadas con una proteína recombinante de Plasmodium vivax. El estudio se realizó en ratones
Científicos obtienen una protección esterilizante en pruebas realizadas con una proteína recombinante de Plasmodium vivax. El estudio se realizó en ratones (imagen: Frontiers in Immunology)
Por Maria Fernanda Ziegler | Agência FAPESP – Una nueva vacuna preclínica contra el paludismo vivax –la forma de malaria con mayor distribución geográfica y mayor prevalencia en toda América– ha sido probada en ratones con una eficacia del 45%, lo que constituye un importante avance en el desarrollo de alternativas de prevención contra esta enfermedad.
De acuerdo con datos de la Organización Mundial de la Salud (OMS) de 2015, los parásitos de la especie Plasmodium vivax fueron responsables por más de 13 millones de casos de malaria en el mundo, y aún no existe un inmunizante disponible contra estos patógenos.
La estrategia de la nueva vacuna se basa en el desarrollo de versiones recombinantes de proteínas encontradas en el esporozoíto, la forma del parásito presente en la glándula salival del mosquito transmisor, que infecta al ser humano. La proteína en cuestión es homóloga a la que está usándose en otra vacuna en estadio más avanzado contra el Plasmodium falciparum, el parásito del paludismo más común en el continente africano.
“Con base en el éxito de esa proteína de P. falciparum, pensamos en intentar algo parecido contra el parásito que acomete a América. Está visto que en África la protección tampoco es alta: va de un 30% a un 40%, pero ha hecho que disminuyan las formas graves de malaria falciparum y ha atrasado el primer episodio de paludismo en niños, disminuyendo así la mortalidad infantil”, dijo Irene Soares, docente de la Facultad de Ciencias Farmacéuticas de la Universidad de São Paulo (FCF-USP), en Brasil, y autora corresponsal del artículo con resultados de la investigación, publicado en la revista Frontiers in Immunology.
La posible vacuna contra el P. falciparum, la RTS,S/ AS01, ha pasado por ensayos clínicos fase III –la investigación clínica se clasifica usualmente en cuatro fases– y recibió un aval de la OMS para la realización de un estudio piloto de implementación. De acuerdo con Soares, dicha vacuna no será para uso general en la población. “Quizá para niños y personas no inmunes, tales como viajeros que van a la región endémica. Es una forma de no padecer esas formas graves de la enfermedad”, dijo Soares.
La iniciativa de desarrollar una vacuna contra el P. vivax surgió de un grupo de científicos del Centro de Terapia Celular y Molecular de la Universidad Federal de São Paulo (Unifesp) y de la FCF-USP. Esta trabajo cuenta con el apoyo por la FAPESP en el marco de un Proyecto Temático, y contó con la colaboración de un equipo internacional, con científicos del Instituto Pasteur (Francia) y de la Agency for Science Technology and Research (Singapur), entre otros.
El P. vivax posee particularidades que dificultan el desarrollo de vacunas. A diferencia del parásito más común del continente africano, la proteína blanco del P. vivax tiene tres formas alélicas, es decir, tres variantes en la naturaleza, llamadas VK210, VK247 y P. vivax-like. Trabajos previos realizados durante las décadas de 1990 y 2000 demostraron que las tres variantes circulan en Brasil, con prevalencia de la VK210.
La proteína circumsporozoíto (CS), la más abundante en la superficie del parásito, es una antigua conocida de la ciencia: fue caracterizada por los científicos brasileños Ruth y Victor Nussenzweig, de la New York University, a partir de la década de 1960.
La molécula está implicada en los estadios iniciales de invasión de células del hígado de los mamíferos infectados. Esto hace que se erija en un blanco importante para anticuerpos y otras células del sistema inmunológico.
“Como la proteína del P. vivax posee tres formas alélicas, elaboramos también una versión híbrida con esas tres variantes reunidas. La misma contiene un fragmento de cada una. En caso de que la vacuna se basase en una sola variante, no protegería contra las otras y no sería abarcadora”, dijo Soares.
Tras producir la proteína fusionada, los investigadores se abocaron a la etapa de inducir anticuerpos contra las tres variantes. Para saber si los anticuerpos reconocían al parásito, el equipo contó con la colaboración de científicos de la Agency for Science Technology and Research, de Singapur.
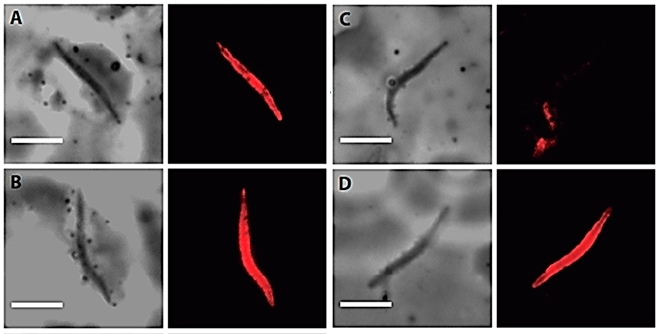
Dicha agencia cedió los esporozoítos extraídos de la saliva del mosquito. En las pruebas, los anticuerpos generados –tanto la mezcla de proteínas como la proteína de fusión– fueron capaces de reconocer a la molécula nativa por inmunofluorescencia.
Las pruebas en animales generaron también otro desafío: los ratones no son infectados por el P. vivax. Para resolver este problema, el equipo contó con la colaboración del Instituto Pasteur (de Francia), donde se testeó un parásito transgénico: el esporozoíto del Plasmodium berghei (que infecta a los ratones) capaz de expresar las repeticiones de la proteína VK210 de P. vivax (Pb/ PvVK210).
“Por eso el artículo cuenta con varios autores de distintos centros de investigación. Fue un trabajo sumamente complejo y con varias etapas”, comentó Soares.
En el laboratorio de Rogerio Amino, investigador brasileño del Instituto Pasteur (Francia) y coautor del estudio, los ratones a los que se les aplicó la fórmula de la vacuna quedaron protegidos contra la infección de esporozoítos quiméricos de P. berghei, al expresar repeticiones de proteínas del circumsporozoíto de P. vivax.
“Fue una colaboración importante. Los animales recibieron tres dosis de la vacuna híbrida y después fueron desafiados con el parásito transgénico. Cuatro de los seis ratones inmunizados se encontraban libres de la infección hasta el décimo día tras el desafío, mientras que todos los animales del grupo de control (no inmunizados) estaban infectados al cabo de cuatro días”, dijo Soares.
De acuerdo con la investigadora, aún faltan etapas por cumplirse hasta que la vacuna se muestre comercialmente interesante y pueda erigirse en una alternativa contra el P. vivax. El inmunizante aún debe probarse en otros mamíferos antes de la etapa de ensayos clínicos, por ejemplo.
La primera autora del artículo, Alba Marina Gimenez, del Centro de Terapia Celular y Molecular de la Unifesp, realizó recientemente una pasantía en la University of Oxford, en el Reino Unido, donde tuvo la oportunidad de testear parásitos transgénicos capaces de expresar cada una de las tres variaciones de la proteína (alelos VK210, VK247 y P. vivax-like). Este trabajo contó con el apoyo de la FAPESP.
Parásitos durmientes
Uno de los grandes desafíos de la nueva vacuna consiste en lograr combatir también a los parásitos que, pasada la fase aguda, permanecen en el hígado en la forma durmiente o latente, y que pueden desencadenar otro episodio de la enfermedad meses después de que el paciente sea infectado. Ésta es otra particularidad del P. vivax.
“Cuando el mosquito pica, algunos de los parásitos inoculados adquieren una forma durmiente o latente (hipnozoítos) en el hígado, mientras los otros causarán la enfermedad. Por ende, cuando se trata a los patógenos en la sangre, los que están ‘durmiendo’ siguen estando listos para atacar nuevamente. El medicamento puede funcionar en el primer momento; empero, al cabo de algunos meses, el parásito puede ‘despertarse’ y regresar a la circulación sanguínea, causando una recaída”, dijo Amino, coautor del estudio.
Amino es también uno de los autores de un trabajo publicado en Trends in Parasitology según el cual una vacuna contra los esporozoítos de P. vivax con moderada eficacia contra la infección primaria, podría reducir sustancialmente la transmisión de hipnozoítos, evitando así las recaídas.
“Sería sumamente interesante si hubiese una vacuna que disminuyese significativamente la cantidad de hipnozoítos, aun cuando no fuera 100% eficaz contra la primoinfección. La vacuna que está desarrollándose contra el P. vivax posee una buena eficacia, pero aún no se ha verificado si puede o no disminuir las recaídas. De funcionar también contra los hipnozoítos; esto será un gran avance”, dijo.
Puede leerse el artículo intitulado Vaccine Containing the Three Allelic Variants of the Plasmodium vivax Circumsporozoite Antigen Induces Protection in Mice after Challenge with a Transgenic Rodent Malaria Parasite (doi: 10.3389/fimmu.2017.01275), de Alba Marina Gimenez, Luciana Chagas Lima, Katia Sanches Françoso, Priscila M. A. Denapoli, Raquel Panatieri, Daniel Y. Bargieri, Jean-Michel Thiberge, Chiara Andolina, Francois Nosten, Laurent Renia, Ruth S. Nussenzweig, Victor Nussenzweig, Rogerio Amino, Mauricio M. Rodrigues e Irene S. Soares, en Frontiers of Immunology, en el siguiente enlace: frontiersin.org/articles/10.3389/fimmu.2017.01275/full.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





