


Imagem tridimensional dos nervos hepáticos obtida pela técnica 3DISCO (imagem: FMRP-USP)
Além de detalhar a morfologia dos nervos hepáticos, pesquisa liderada por brasileiros mostra que aumento de açúcar é ativado por uma proteína chamada CREB
Além de detalhar a morfologia dos nervos hepáticos, pesquisa liderada por brasileiros mostra que aumento de açúcar é ativado por uma proteína chamada CREB
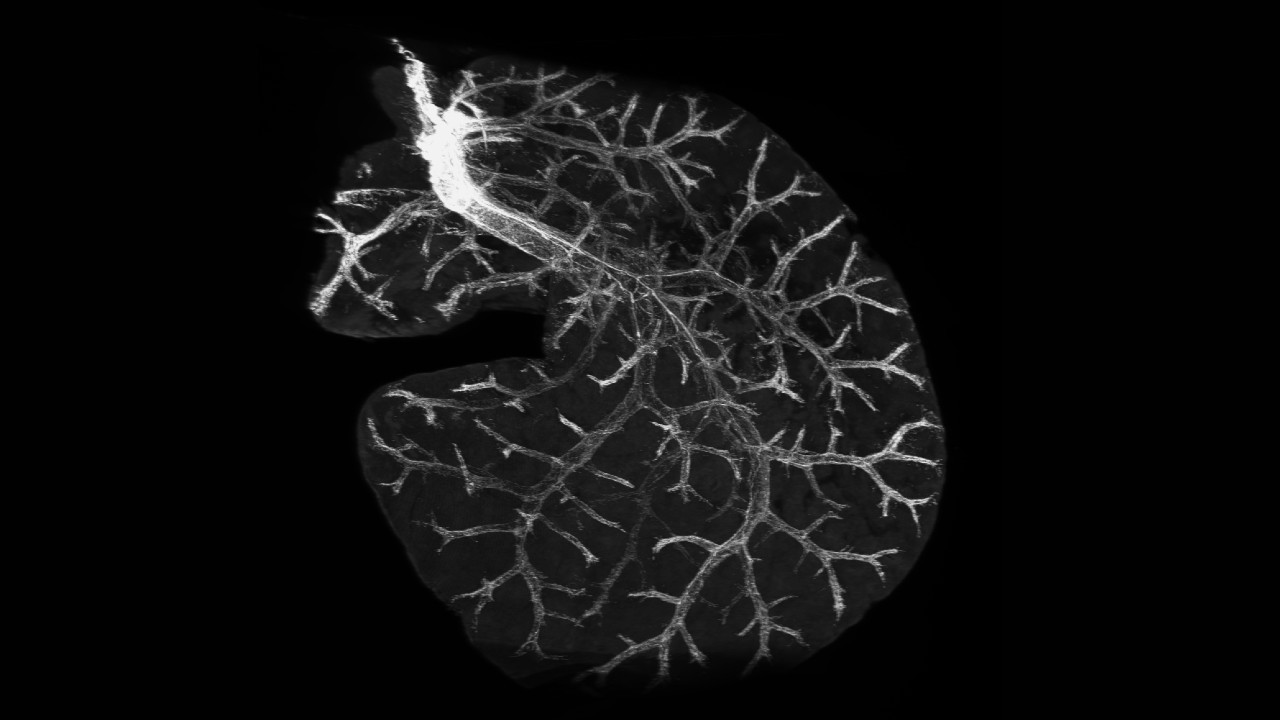
Imagem tridimensional dos nervos hepáticos obtida pela técnica 3DISCO (imagem: FMRP-USP)
Luciana Constantino | Agência FAPESP – Uma pesquisa liderada por brasileiros descreveu detalhadamente a morfologia dos nervos no fígado e como eles controlam a produção de glicose em situação de estresse do organismo. Esse processo, conhecido como gliconeogênese hepática, é vital na manutenção da glicemia durante o jejum e em ocasiões de alta demanda energética.
Publicado na revista científica Metabolism, o estudo foi feito em camundongos. Mostrou que, em resposta ao frio, os nervos simpáticos que liberam noradrenalina no fígado ajudaram a aumentar o açúcar no sangue ao ativar o processo de produção de glicose. Essa ativação envolveu moléculas específicas – a proteína CREB e seu ativador CRTC2 –, pouco estudadas nesse contexto.
A noradrenalina (ou norepinefrina) é um neurotransmissor fundamental na rápida resposta do corpo humano a situações de estresse ou perigo, aumentando a frequência cardíaca, a pressão arterial e a liberação de glicose a partir de reservas de energia. Atualmente, na literatura científica, a maior parte dos estudos sobre a regulação da produção de glicose pelo fígado tem como alvo a ação de hormônios do pâncreas e das glândulas adrenais.
A compreensão desses mecanismos é crucial para desvendar os processos fisiológicos desordenados que levam a doenças metabólicas, entre elas diabetes e obesidade. Por isso, os achados da pesquisa podem abrir caminhos para novos estudos focados no tema, especialmente em situações de alterações do sistema nervoso simpático, como a hipertensão e a esteatose (acúmulo de gordura) hepática.
“A originalidade do nosso trabalho foi mostrar que o sistema nervoso central, por meio de nervos simpáticos, pode controlar CREB e ativar de novo a produção hepática de glicose em uma situação de demanda energética. Descrevemos a anatomia da inervação que chega ao fígado usando uma metodologia inédita no Brasil”, explica à Agência FAPESP o professor Luiz Carlos Navegantes, do Departamento de Fisiologia da Faculdade de Medicina de Ribeirão Preto da Universidade de São Paulo (FMRP-USP), autor correspondente do artigo.
Os pesquisadores usaram uma técnica chamada 3DISCO (sigla em inglês para three-dimensional imaging of solvent-cleared organs) – um método histológico que torna as amostras biológicas mais transparentes usando uma série de solventes orgânicos, permitindo assim uma imagem tridimensional com os nervos em destaque.
O trabalho recebeu apoio da FAPESP por meio de um Projeto Temático e de bolsas de mestrado e doutorado (19/05900-6, 19/26583-9 e 21/05848-4) concedidas ao biólogo Henrique Jorge Novaes Morgan, primeiro autor do artigo, que venceu o Prêmio Álvaro Osório de Almeida, concedido pela Sociedade Brasileira de Fisiologia em 2021.
Também participaram do estudo pesquisadores da Universidade de Oxford (Reino Unido), do Instituto Francis Crick (em Londres) e o professor Marc Montminy, do Salk Institute for Biological Studies (Estados Unidos), que “descobriu” CREB e elucidou seu papel como regulador do metabolismo energético, revelando potenciais alvos de medicamentos para resistência à insulina, diabetes e obesidade.
Metodologia
Usando o imunomapeamento em 3D, os cientistas analisaram a distribuição dos nervos simpáticos no fígado dos camundongos, observando-se uma densa inervação composta por fibras nervosas primárias espessas, que se ramificam, mas não alcançam diretamente o hepatócito (célula do fígado).
Para investigar o papel fisiológico da inervação, os animais foram expostos a baixas temperaturas (4°C) por até seis horas. O estresse pelo frio ativou CREB/CRTC2, por meio de um sinal de cálcio (Ca2+), para garantir o fornecimento de glicose para os músculos, ajudando a manter o corpo dos roedores aquecido.
“Dando continuidade aos estudos pioneiros do professor Renato Hélios Migliorini, fundador de nosso laboratório, que na década de 1980 demonstrou que o sistema nervoso era capaz de ativar a gliconeogênese, precisávamos entender o que acontecia em nível molecular. Por isso, analisamos animais dos quais tiramos essa inervação do fígado por meio de dois métodos diferentes – um químico e um cirúrgico – e em camundongos transgênicos sem o CRTC2. Nesses casos, não houve a gliconeogênese em resposta ao frio, ou seja, sem os nervos ou sem o coativador de CREB o roedor não consegue produzir a glicose em situação de estresse. Com esses resultados, estamos acrescentando um novo componente nas pesquisas”, completa Navegantes.
O artigo Hepatic noradrenergic innervation acts via CREB/CRTC2 to activate gluconeogenesis during cold pode ser lido em www.sciencedirect.com/science/article/pii/S0026049524001677.
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





