


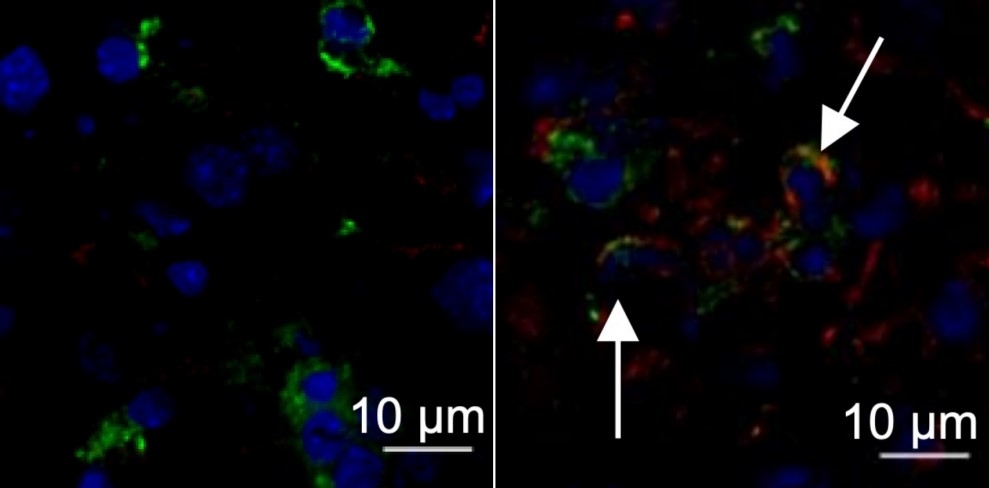
A la izquierda, en azul, núcleos de células de hígado de un ratón sano; a la derecha, el órgano de un animal infectado con el virus de la hepatitis murina con flechas que señalan la expresión de la proteína TMEM176D, en rojo (imagen: Maite D. Veja et. al.)
Se trata de un tipo de tratamiento conocido como inhibidor de checkpoint inmunológico y exhibió beneficios en células de pacientes internados en UTI tras infectarse con el SARS-CoV-2, como así también en ratones infectados con un betacoronavirus similar. La investigación referente salió publicada en Science Advances
Se trata de un tipo de tratamiento conocido como inhibidor de checkpoint inmunológico y exhibió beneficios en células de pacientes internados en UTI tras infectarse con el SARS-CoV-2, como así también en ratones infectados con un betacoronavirus similar. La investigación referente salió publicada en Science Advances
A la izquierda, en azul, núcleos de células de hígado de un ratón sano; a la derecha, el órgano de un animal infectado con el virus de la hepatitis murina con flechas que señalan la expresión de la proteína TMEM176D, en rojo (imagen: Maite D. Veja et. al.)
Por André Julião | Agência FAPESP – Un estudio publicado en la revista Science Advances sugiere que un tipo de tratamiento conocido como inhibidor de checkpoint inmunológico –aplicado contra ciertos tipos de cánceres– puede ser beneficioso en algunos casos graves de COVID-19. Los creadores de este tipo de terapia, que posee la capacidad de reactivar el sistema inmunitario, ganaron el Premio Nobel de Medicina en 2018.
Las conclusiones del artículo se basan en experimentos realizados con células de pacientes que debieron ser internados en Unidades de Terapia Intensiva (UTI) tras infectarse con el SARS-CoV-2, y con ratones infectados con otro betacoronavirus, el MHV-A59 (el virus de la hepatitis murina A59).
“Uno de los checkpoints inmunológicos conocidos y con el cual trabajamos en el estudio es el PD-1. Este les señala a los linfocitos T [un tipo de leucocitos] que deben dejar de responder ante la infección al cabo de un tiempo, para que no se produzca una respuesta exacerbada. Pero en un contexto de cáncer, sepsis o COVID-19 grave, el PD-1 hace que los linfocitos T dejen de funcionar antes incluso de que se disipe la enfermedad. Por eso hay que bloquearlo”, explica Pedro Moraes-Vieira, uno de los coordinadores del estudio y docente del Instituto de Biología de la Universidad de Campinas (IB-Unicamp), en el estado de São Paulo, Brasil, que cuenta con el apoyo de la FAPESP.
Uno de los autores de este trabajo es Gustavo Gastão Davanzo, doctorando en el IB-Unicamp y becario de la FAPESP.
“Aun cuando son tratamientos de costo sumamente elevado, el hecho de que no haya más tantos pacientes graves como al comienzo de la pandemia nos lleva a creer que esta sería una de las opciones viables, en caso de que nuevos estudios demuestren que esta terapia es segura con pacientes con COVID-19”, afirma Moraes-Vieira.
El coronavirus del ratón
La hipótesis del estudio surgió cuando científicos uruguayos –coautores del artículo– observaron que ratones que no expresaban la proteína TMEM176D exhibían respuestas más agudas a la infección con el MHV-A59. Esa proteína tiene la función de regular el denominado inflamasoma, un complejo proteico existente dentro de las células de defensa que controla la inflamación en un organismo con el objetivo de destruir amenazas tales como tumores, virus y bacterias.
Sin la proteína TMEM176D, el inflamasoma se activa más aún, con una mayor liberación de citoquinas inflamatorias como la interleuquina-1 beta (IL-1β), cuyo papel es conocido en el COVID-19 grave (lea más en: agencia.fapesp.br/34747/).
“Esta liberación excesiva de IL-1β deriva en una disfunción de los linfocitos T: es lo que denominamos como agotamiento de esas células de defensa. Se activan tanto que ya no logran responder adecuadamente. Es algo muy común en enfermedades virales crónicas como el COVID-19 grave, algo que ya habíamos observado en un trabajo que realizamos al comienzo de la pandemia”, comenta Moraes-Vieira.
El trabajo al que el investigador hace referencia salió publicado en 2020 en Cell Metabolism y hasta la fecha se ubica entre los artículos más citados de la revista en los últimos tres años. Y motivó la consulta del equipo uruguayo para proponer la colaboración (lea más en: agencia.fapesp.br/33314/).
En las pruebas con ratones, el tratamiento con el inhibidor de PD-1 logró restaurar la función de los linfocitos T. Asimismo, los investigadores tuvieron acceso a la sangre de donantes sanos y de pacientes con COVID-19 internados en dos instituciones de la ciudad de Montevideo, en Uruguay.
Los experimentos con células sanas, posteriormente infectadas con el SARS-CoV-2, se realizaron en el Laboratorio de Estudios de Virus Emergentes (LEVE) bajo la coordinación de José Luiz Proença Módena, docente del IB-Unicamp apoyado por la FAPESP y coautor del artículo.
En los test con muestras de pacientes, solamente las células provenientes de internados en UTI se beneficiaron con la administración del atezolizumab, el fármaco inhibidor del PD-1 utilizado en el estudio. Esto sucede precisamente porque en esos pacientes se produce una activación exacerbada del inflamasoma, lo que lleva a ese perfil de agotamiento y disfunción de la inmunidad adaptativa.
Los investigadores advierten que estos resultados deben observarse con cautela. Estudios con pacientes con cáncer que ya hacían uso de este tratamiento antes de contraer COVID-19 no mostraron beneficios o incluso redundaron en una asociación negativa.
En uno de ellos, la administración de la terapia antes de la infección viral no generó una mejoría del cuadro de COVID-19. En otro trabajo, que comprendió un seguimiento con 423 pacientes, hubo más casos de hospitalización y severidad de la enfermedad entre aquellos a los que se les había administrado el inhibidor. Por otra parte, un estudio clínico con inhibidores de PD-1 en pacientes con sepsis mostró que la terapia es segura. Por ende, serán necesarios nuevos estudios para conocer mejor los efectos del tratamiento en el contexto del COVID-19.
Puede leerse el artículo intitulado PD-1/PD-L1 blockade abrogates a dysfunctional innate-adaptive immune axis in critical β-coronavirus disease en el siguiente enlace: www.science.org/doi/10.1126/sciadv.abn6545.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





