


Estrutura tridimensional da enzima metamórfica: sob estresse oxidativo, partes essenciais se tornam desorganizadas, impedindo o encaixe do substrato e interrompendo a reação bioquímica; quando o ambiente volta a ser favorável, a estrutura se reorganiza e a atividade é restaurada (imagem: Gustavo Henrique Barreto Gimenis/CNPEM)
Estudo conduzido no CNPEM com apoio da FAPESP revela mecanismo em enzima da microbiota de capivara
Estudo conduzido no CNPEM com apoio da FAPESP revela mecanismo em enzima da microbiota de capivara
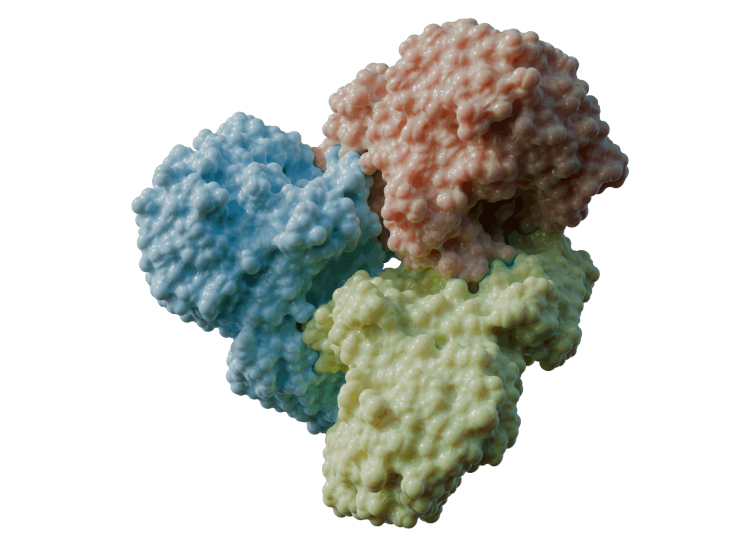
Estrutura tridimensional da enzima metamórfica: sob estresse oxidativo, partes essenciais se tornam desorganizadas, impedindo o encaixe do substrato e interrompendo a reação bioquímica; quando o ambiente volta a ser favorável, a estrutura se reorganiza e a atividade é restaurada (imagem: Gustavo Henrique Barreto Gimenis/CNPEM)
Agência FAPESP – Cientistas do Centro Nacional de Pesquisa em Energia e Materiais (CNPEM) identificaram um mecanismo molecular que controla a obtenção de energia de carboidratos pela microbiota intestinal de capivaras. A descoberta abre caminho para desenvolver enzimas com atividade modulável ao ambiente, com aplicações em áreas como biorrefinarias, biotecnologia ambiental, biossensores e na produção de prebióticos voltados à promoção da saúde intestinal.
Financiado pela FAPESP (21/04891-3, 22/03059-5, 21/09793-0, 24/15257-1, 22/06298-0 e 22/09386-8), o estudo faz parte de uma linha de pesquisa de valorização da biodiversidade brasileira, com a descoberta de enzimas para diferentes aplicações biotecnológicas, da agricultura e nutrição animal à energia sustentável.
“É como se a enzima tivesse um interruptor molecular de liga e desliga embutido na própria estrutura, que responde diretamente às condições químicas do ambiente”, explicou Marcele Martins, principal autora do artigo, à Assessoria de Imprensa do CNPEM. Segundo ela, o mecanismo é mediado por um sítio ativo moldável – maleável, que se ajusta de acordo com o meio –, capaz de regular dinamicamente a atividade da proteína.
Com isso, essas enzimas oferecem uma base promissora para a engenharia de sistemas enzimáticos redox-responsivos, podendo ser usadas em biorrefinarias para controle do processamento de biomassa e na produção de prebióticos.
O estudo, publicado na revista Nature Communications, foi realizado em colaboração com grupos do Centre National de la Recherche Scientifique e da Université Grenoble-Alpes (França), da Universidade Estadual de Campinas (Unicamp) e da Universidade de Cambridge (Reino Unido).
Identificação da enzima
A descoberta teve origem na investigação de microrganismos associados à biodiversidade brasileira, campo ainda pouco explorado. Os pesquisadores identificaram a enzima em bactérias da microbiota intestinal da capivara que, sob condições de estresse oxidativo, se desorganiza estruturalmente e interrompe a função digestiva; quando o ambiente se estabiliza, a enzima recupera sua forma original e volta a atuar normalmente. Todo o processo é reversível, o que é raro nesse tipo de enzima (leia mais em: agencia.fapesp.br/38486).
Para desvendar esse funcionamento, a equipe combinou técnicas experimentais avançadas que permitiram observar a estrutura da enzima tanto no estado ativo quanto no inativo. Os resultados mostraram que a alternância entre os dois estados depende da formação temporária de uma ligação química interna que atua como uma chave estrutural para controlar a função da enzima.
“Esse tipo de mecanismo ajuda a explicar como microrganismos se adaptam a ambientes variáveis e inspira novas estratégias para o uso de enzimas em processos tecnológicos”, destaca Martins.
O artigo A disulfide redox switch mechanism regulates glycoside hydrolase function pode ser lido em: nature.com/articles/s41467-025-67225-2.
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





