


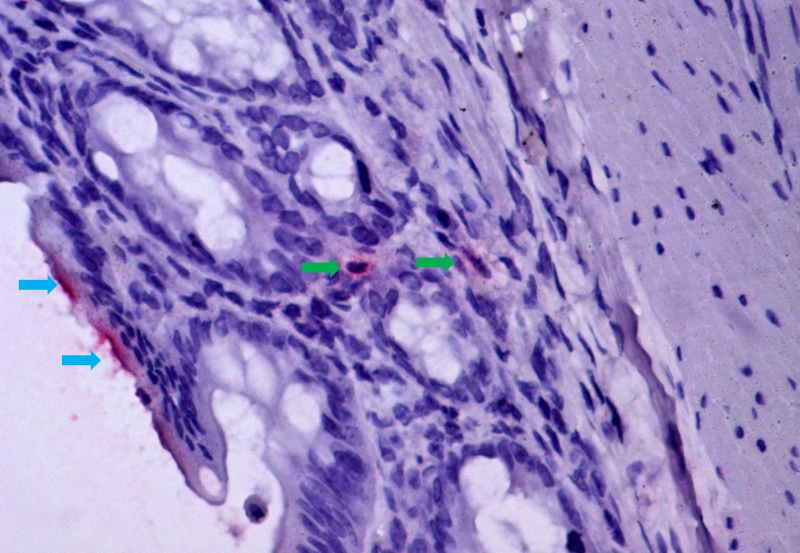
Mucosa intestinal de hámster infectado por el virus de la fiebre amarilla, mostrando isquemia y translocación bacteriana, mecanismo de paso de bacterias y sus productos (marcados en rojo, por inmunohistoquímica) desde el lumen intestinal (flechas azules) hacia la mucosa intestinal (flechas verdes), alcanzando el torrente sanguíneo. El mismo mecanismo de lesión ocurre en humanos con fiebre amarilla fatal (imagen: Amaro Nunes Duarte Neto/HC-FM-USP)
Investigadores de la Universidad de São Paulo y de la Universidad de Wisconsin-Madison constataron que la hemorragia en el intestino durante la progresión de casos graves de la enfermedad causa infección sistémica, contribuyendo al empeoramiento del cuadro provocado por la infección viral
Investigadores de la Universidad de São Paulo y de la Universidad de Wisconsin-Madison constataron que la hemorragia en el intestino durante la progresión de casos graves de la enfermedad causa infección sistémica, contribuyendo al empeoramiento del cuadro provocado por la infección viral
Mucosa intestinal de hámster infectado por el virus de la fiebre amarilla, mostrando isquemia y translocación bacteriana, mecanismo de paso de bacterias y sus productos (marcados en rojo, por inmunohistoquímica) desde el lumen intestinal (flechas azules) hacia la mucosa intestinal (flechas verdes), alcanzando el torrente sanguíneo. El mismo mecanismo de lesión ocurre en humanos con fiebre amarilla fatal (imagen: Amaro Nunes Duarte Neto/HC-FM-USP)
Por Elton Alisson | Agência FAPESP – Además de afectar principalmente el hígado y, por ello, ser considerada una enfermedad hepática, la fiebre amarilla compromete, en su fase aguda, diversos otros órganos, como riñones, corazón, cerebro y pulmones.
Un estudio realizado por investigadores de las universidades de São Paulo (USP), en Brasil, y de Wisconsin-Madison, en Estados Unidos, indicó que, durante la progresión de los casos graves de la enfermedad —en los que surgen complicaciones que pueden llevar a la muerte—, también se produce hemorragia en la mucosa intestinal. Este daño gastrointestinal permite que bacterias del interior del órgano ingresen al torrente sanguíneo y alcancen el hígado, causando una infección sistémica generalizada —la sepsis—, que agrava el cuadro clínico inicialmente provocado por el virus.
Los resultados del trabajo, apoyado por la FAPESP, sugieren que el daño gastrointestinal es un factor clave que diferencia los casos fatales de los tratables y puede orientar nuevas estrategias terapéuticas centradas en la prevención de la sepsis bacteriana. Los hallazgos fueron descritos en un artículo publicado en el Journal of Infectious Diseases.
“Observamos que la disminución del suministro sanguíneo en el intestino, que denominamos isquemia mesentérica, termina permitiendo el paso de productos bacterianos del órgano —que posee la mayor concentración de la microbiota humana— hacia la sangre de los pacientes que desarrollaron la forma más grave de fiebre amarilla”, afirma a la Agência FAPESP Esper Kallás, profesor de la Facultad de Medicina (FM) de la USP y uno de los autores del estudio.
“Esto termina generando un aumento de neutrófilos en la sangre [tipo de glóbulo blanco que constituye la primera línea de defensa contra bacterias y hongos]”, explica el investigador, quien también es director del Instituto Butantan.
El enigma de los neutrófilos
El investigador y sus colaboradores, vinculados al Laboratorio de Alergia e Inmunopatología Clínica de la FM-USP, ya habían observado que los pacientes con fiebre amarilla y aumento del número de neutrófilos presentaban mayor mortalidad. Publicado en un artículo anterior, el hallazgo intrigó al grupo, ya que los neutrófilos se asocian comúnmente a la respuesta inmunológica frente a infecciones bacterianas, mientras que la fiebre amarilla es una enfermedad viral.
Para investigar las causas de esta neutrofilia, en 2020 iniciaron un estudio con pacientes que presentaron la forma más grave de la enfermedad. “Una de las hipótesis planteadas fue que la propia cascada inflamatoria podría conducir a la neutrofilia. Otra posibilidad sería un reflejo de alteración medular inducida por el virus, pero eso no encajaba bien”, relata Kallás.
La hipótesis más plausible fue que la neutrofilia sería causada por un proceso inflamatorio desencadenado en el intestino debido a una isquemia. Las bacterias estarían atravesando la barrera intestinal e ingresando al torrente sanguíneo, provocando una inflamación acentuada que empeoraba el cuadro y conducía al fallecimiento.
Marcador biológico
Con el fin de identificar posibles marcadores biológicos asociados a este proceso de translocación bacteriana, el investigador Mateus Vailant Thomazella, bajo la dirección de Kallás, analizó, con beca de la FAPESP, muestras de plasma de 90 pacientes con cuadro grave internados en el Hospital de Clínicas de la FM-USP y en el hospital del Instituto de Infectología Emílio Ribas entre 2018 y 2019 – de los cuales 27 fallecieron.
El análisis del plasma sanguíneo de los pacientes que murieron indicó que la I-FABP (sigla en inglés de proteína ligadora de ácidos grasos intestinal) desempeña un papel importante en el pronóstico de la enfermedad, actuando como biomarcador específico de daño intestinal. Las concentraciones plasmáticas de I-FABP fueron significativamente más elevadas en los casos fatales.
“La I-FABP es un marcador estrechamente asociado a la lesión de los enterocitos, células que constituyen la mucosa intestinal. Cuando se producen daños en esta mucosa, los niveles de esta proteína aumentan en el plasma”, explica Thomazella.
Observaciones en autopsias
El daño en la mucosa intestinal también venía siendo observado por Amaro Nunes Duarte, profesor del Departamento de Patología de la FM-USP. Al realizar autopsias durante la epidemia en São Paulo (2018-2019), Duarte notó hemorragia en la pared intestinal e isquemia del lecho esplácnico – la red de vasos que irriga los órganos abdominales.
“Inicialmente, estas observaciones fueron tratadas como impresiones anatómicas del patólogo, pero al analizar las láminas constaté lesión vascular en los intestinos y en el estómago, característica de la falta de irrigación. La lesión vascular de la mucosa gastrointestinal permite el paso de bacterias del lumen intestinal hacia la sangre y el hígado, agravando el daño inicial provocado por el virus de la fiebre amarilla y conduciendo a la muerte”, explica Duarte.
Para validar los hallazgos, los investigadores de la USP se asociaron con el profesor Adam Bailey, de la Universidad de Wisconsin-Madison, quien desarrolló un modelo experimental de hámster infectado por el virus. Los análisis de los tejidos animales evidenciaron un cuadro similar al humano, con hemorragias y trombos en la pared intestinal.
“La entrada de bacterias en la sangre de los animales mostró que la translocación es un mecanismo progresivo en la evolución de la fiebre amarilla grave”, afirma Duarte. Los investigadores pretenden ahora analizar muestras de pulmones de pacientes fallecidos para comprender los efectos de esta translocación en el órgano.
El artículo Mesenteric ischemia and bacterial translocation precipitate the intoxication phase of yellow fever puede leerse en: academic.oup.com/jid/advance-article-abstract/doi/10.1093/infdis/jiaf483/8261590.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





