


En pruebas con ratones, un biomaterial mantuvo vivas a las células mesenquimales y redujo el tamaño de una lesión isquémica. Este procedimiento puede ayudar en el tratamiento de lesiones cerebrales aún mayores (imágenes cedidas por los científicos)
En pruebas con ratones, un biomaterial mantuvo vivas a las células mesenquimales y redujo el tamaño de una lesión isquémica. Este procedimiento puede ayudar en el tratamiento de lesiones cerebrales aún mayores
En pruebas con ratones, un biomaterial mantuvo vivas a las células mesenquimales y redujo el tamaño de una lesión isquémica. Este procedimiento puede ayudar en el tratamiento de lesiones cerebrales aún mayores
En pruebas con ratones, un biomaterial mantuvo vivas a las células mesenquimales y redujo el tamaño de una lesión isquémica. Este procedimiento puede ayudar en el tratamiento de lesiones cerebrales aún mayores (imágenes cedidas por los científicos)
Por André Julião | Agência FAPESP – Científicos han logrado disminuir el tamaño de lesiones provocadas por isquemia cerebral en cerebros de ratones mediante la aplicación de células madre.
Esas células madre mesenquimales –que originan tejidos–, extraídas de la médula ósea de los animales, se encontraban en un soporte elaborado con un material que no sólo permitió su supervivencia y su multiplicación, sino que también impidió que migrasen hacia otras áreas del cerebro, tal como es común que ocurra cuando se las implanta directamente en la lesión.
Esta técnica puede ayudar en la recuperación de víctimas de accidentes cerebrovasculares (ACVs) isquémicos, cuando una vena del cerebro es bloqueada (trombo) y la parte del cerebro que deja de ser irrigada padece la muerte de sus neuronas. La isquemia puede causar secuelas graves, tales como pérdidas de movimientos, e incluso llevar a la muerte.
Actualmente existen dos procedimientos posibles con los pacientes que sufren un ACV isquémico. Uno de ellos es la terapia de recanalización intravascular (trombólisis), cuando se aplica un medicamento activador de plasminógeno (rtPA) que deshace el trombo. La otra opción es un cateterismo para desobstruir mecánicamente el vaso, para que la sangre vuelva a circular.
No obstante, estos tratamientos sólo tienen eficacia cuando se los aplica en un plazo máximo de cuatro horas y media después del ACV. Posteriormente, la muerte celular es irreversible. La nueva técnica surge como una posibilidad de tratamiento aun después de ese lapso de tiempo.
Los resultados del estudio salieron publicados en Nanomedicine: Nanotechnology, Biology, and Medicine, en un artículo cuya primera autora es Laura Zamproni, y forma parte de su doctorado, realizado con beca de la FAPESP en la Escuela Paulista de Medicina de la Universidad Federal de São Paulo (EPM-Unifesp), en Brasil, donde actualmente realiza su posdoctorado.
Zamproni es médica neuróloga del Hospital São Paulo, de la Unifesp. Su trabajo cotidiano suscitó su curiosidad con respecto a la investigación básica. “El procedimiento que existe actualmente para la isquemia tiene sus beneficios, pero incluso cuando se lo realiza dentro de ese corto lapso de tiempo, puede dejar secuelas y algún déficit cognitivo”, dijo.
No es la primera vez que científicos intentan utilizar células madre para recuperar un área dañada del cerebro de ratones o ratas. Pero en los ensayos anteriores, cuando se las implantó directamente en la lesión, casi ninguna célula sobrevivió (un 0,005%). Las que sobrevivieron migraron hacia otras zonas del cerebro. Cuando se las inyectó en el torrente sanguíneo, permanecieron retenidas en los riñones o en los pulmones de los animales utilizados en el experimento.
Lo que marcó la diferencia en este caso fue el uso de un material que, aparte de ser biocompatible (no tóxico), aumenta la supervivencia de las células madre y hace que éstas permanezcan en el área de la lesión, con lo cual disminuye la inflamación. Al cabo de algunos meses, con el área en gran medida recuperada, el material es totalmente absorbido por el cuerpo.
El desarrollo de esta novedad estuvo a cargo de los ingenieros biomédicos Anderson de Oliveira Lobo y Fernanda Roberta Marciano, de la Universidade Brasil. Ambos contaron con ayudas del Programa Jóvenes Investigadores de la FAPESP.
La fibra que desarrollaron es de un polímero orgánico, el ácido poliláctico. Se forma cuando se la dispone en un aparato que calienta el material y gira a alta velocidad, como una máquina de algodón de azúcar. El “algodón” que se forma posee fibras altamente porosas.
Para este estudio, las células madre mesenquimales se extrajeron de la médula ósea de ratones y se las cultivó en placa de Petri. Luego se las depositó en el material.
“Cuando ese material con las células madre mesenquimales se implantó en un cerebro lesionado, la lesión se redujo a un tercio del tamaño que tendría de no haberse efectuado la intervención”, dijo Marimélia Porcionatto, docente de la EPM-Unifesp y coordinadora del estudio.
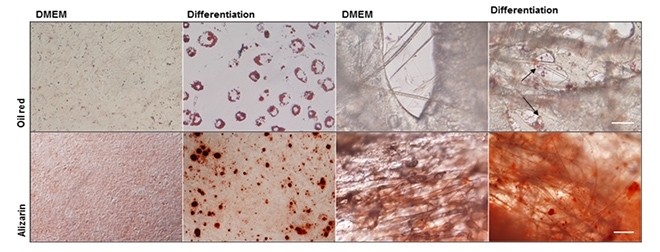
“Anteriormente realizamos varias pruebas para demostrar que las células no pierden sus características biológicas, tales como la diferenciación y la proliferación. Esto es importante, pues no podemos utilizar como soporte un material que altere en demasía las características de las células”, dijo Porcionatto.
Las fibras con las células madre fueron entonces dispuestas sobre la lesión y se les realizó un seguimiento durante 30 días. Los investigadores observaron que funcionan mejor en el material que en la laminillla donde normalmente se las cultiva en laboratorio.
Las pruebas mostraron que éstas producen en mayor cantidad una citocina llamada CXCL12, que atrae a las células hacia la zona. Asimismo, producen también más proteínas conocidas como integrinas, que hacen que las células madre se adhieran al área donde se encuentran.
“Es como si las células madre mesenquimales estuviesen produciendo un ambiente apropiado para quedarse. Aún no sabemos qué es lo que causa esto en ese material, pero es sumamente interesante ver de qué manera un material no biológico interfiere en el comportamiento de las células”, dijo Porcionatto.
Los investigadores ahora pretenden poner a prueba esta técnica con células madre en traumatismos craneoencefálicos, cuando se produce una pérdida de parte del cerebro.
“En la actualidad, cuando se pierde masa encefálica, se controla la hemorragia y se procede a realizar una cirugía, pero lo que se perdió queda perdido. No hay manera de mejorarlo. Éste podría ser un nuevo tratamiento”, dijo Zamproni.
Para eso los investigadores pretenden valerse de la bioimpresión, recreando la parte perdida del cerebro en el mismo formato con una impresora 3D. Para ello, están abocados a la búsqueda de otro biomaterial que pueda también moldearse, aparte de poseer las propiedades del ácido poliláctico.
El artículo intitulado Rotary jet-spun porous microfibers as scaffolds for stem cells delivery to central nervous system injury (doi: 10.1016/j.nano.2018.08.014), de Laura N. Zamproni, Marco A. Grinet, Mayara V. Mundim, Marcella B. Reis, Layla T. Galindo, Fernanda R. Marciano, Anderson O. Lobo y Marimelia Porcionatto, se encuentra disponible en el siguiente enlace: www.sciencedirect.com/science/article/pii/S1549963418305203.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





