

Científicos de un Centro de Investigaciones apoyado por la FAPESP detectaron una alteración no heredada en células de la sangre de una persona con síndrome de deficiencia de GATA2 que puede haber impedido la falencia de la médula ósea y otras manifestaciones clínicas (tejido pulmonar del paciente con síndrome de deficiencia de GATA2 con proteinólisis alveolar e infiltración inflamatoria linfoplasmacítica; imagen: CTC)
Científicos de un Centro de Investigaciones apoyado por la FAPESP detectaron una alteración no heredada en células de la sangre de una persona con síndrome de deficiencia de GATA2 que puede haber impedido la falencia de la médula ósea y otras manifestaciones clínicas.
Científicos de un Centro de Investigaciones apoyado por la FAPESP detectaron una alteración no heredada en células de la sangre de una persona con síndrome de deficiencia de GATA2 que puede haber impedido la falencia de la médula ósea y otras manifestaciones clínicas.
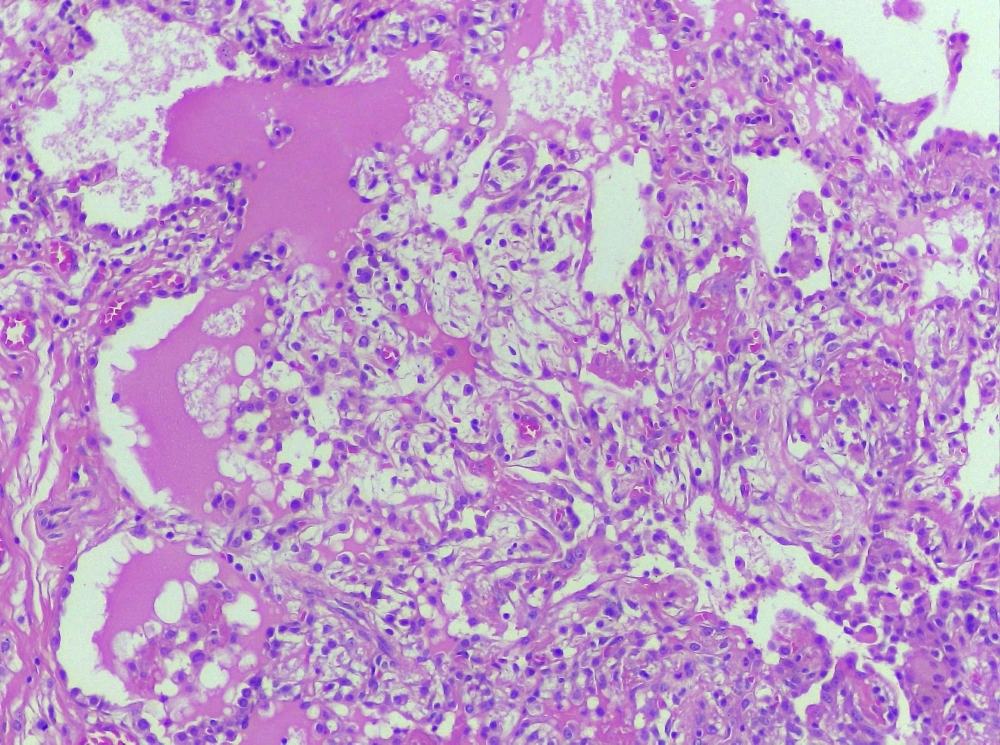
Científicos de un Centro de Investigaciones apoyado por la FAPESP detectaron una alteración no heredada en células de la sangre de una persona con síndrome de deficiencia de GATA2 que puede haber impedido la falencia de la médula ósea y otras manifestaciones clínicas (tejido pulmonar del paciente con síndrome de deficiencia de GATA2 con proteinólisis alveolar e infiltración inflamatoria linfoplasmacítica; imagen: CTC)
Por Elton Alisson | Agência FAPESP – Científicos vinculados al Centro de Terapia Celular (CTC), hospedado en el campus de la Universidad de São Paulo (USP) de la ciudad de Ribeirão Preto, en Brasil, detectaron por primera vez una mutación no hereditaria en células de la sangre de un paciente con síndrome de deficiencia de GATA2, una enfermedad rara causada por una mutación heredada en el gen que codifica a la proteína homónima.
La mutación no hereditaria (somática) puede haber actuado como una terapia génica natural, al impedir que el proceso de renovación celular de la sangre (hematopoyesis) se viese perjudicado por la enfermedad y que el paciente desarrollase las manifestaciones clínicas típicas, tales como falencia de la médula ósea, sordera y obstrucción del sistema linfático (linfedema), según estiman los investigadores.
Los resultados de este estudio, publicado en la revista Blood, y destacado en su portada y en el editorial, abren una perspectiva de utilización de la terapia génica y modificación de la asesoría genética de las familias portadoras de la referida enfermedad hereditaria.
“Al identificar a un paciente con la mutación germinativa [heredada] en la proteína GATA2, se hace necesario estudiar a la familia, pues puede haber casos silenciosos”, le dice a Agência FAPESP Luiz Fernando Bazzo Catto, primer autor del estudio.
Bazzo Catto cursa su doctorado en la USP de Ribeirão Preto bajo la dirección de tesis del profesor Rodrigo Calado, coautor del artículo e integrante del CTC, un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la FAPESP.
El paciente fue identificado en el marco de la atención médica de sus dos hijos en el Hemocentro del Hospital de Clínicas mantenido por la Facultad de Medicina de Ribeirão Preto (FMRP) de la USP.
A uno de los hijos se le diagnosticó anemia aplástica moderada −cuando el organismo deja de producir una cantidad suficiente de nuevas células sanguíneas– y artritis psoriática. El cuadro de falencia de la médula ósea y la consiguiente merma de la producción de células del sistema inmunológico, tales como linfocitos y monocitos, se agravaron durante los cinco años posteriores, y el paciente falleció a los 27 años debido a una infección pulmonar.
La secuenciación del ADN con leucocitos y fibroblastos de la piel del joven tras su muerte reveló que tenía una mutación germinativa en el gen de la GATA2, y confirmó el diagnóstico de deficiencia de la proteína.
Los resultados de la secuenciación de leucocitos y fibroblastos de la piel del segundo hijo, atendido en la institución por primera vez a los 25 años y con una historia clínica de infecciones pulmonares recurrentes, hipotiroidismo, trombosis y sordera, también indicaron la presencia de la mutación germinativa en el mismo sitio del gen.
A los efectos de identificar de cuál de los progenitores les heredaron la mutación, los investigadores secuenciaron el ADN de la madre y del padre de ambos hermanos. Y los resultados indicaron que la madre no tenía la alteración, en tanto que el padre, de 61 años, poseía una mutación idéntica a la de los hijos, tanto en los espermatozoides como en fibroblastos de la piel. Sin embargo, no exhibía manifestaciones clínicas de la enfermedad y los conteos sanguíneos y de linfocitos se ubicaban dentro del rango normal.
“Con ese descubrimiento, surgió la duda acerca de si el padre les había transmitido la mutación a los hijos o si la había adquirido, pero no se las pasó a ellos”, comenta Bazzo Catto.
Para dilucidar este interrogante, se secuenció el ADN de la médula ósea del padre, a fin de estimar el porcentaje de células de la sangre normales que hizo que no exhibiese manifestaciones clínicas de la deficiencia de GATA2, y el de remanentes similares a las de los hijos.
Los resultados de la secuenciación de última generación mostraron que el 93% de los leucocitos del padre tenían la mutación somática que dota de protección contra las manifestaciones clínicas de la deficiencia de GATA2, en tanto que el 7% restante de ellos portaban la mutación asociada a la enfermedad rara. “Ese 7% restante es un remanente del clon original”, explica Bazzo Catto.
Las perspectivas de tratamiento
Los investigadores también evaluaron si la mutación somática detectada en el padre era capaz de inducir la producción de células normales de la sangre durante un largo período. Para ello secuenciaron linfocitos T, que poseen una larga vida útil.
Los resultados de los análisis mostraron que la mutación somática se concretó al comienzo de la vida de esas células y del desarrollo de las células madre hematopoyéticas, con potencial para formar sangre.
“Es muy probable que el padre haya adquirido esta mutación somática en la sangre hace mucho tiempo”, estima Bazzo Catto.
En tanto, para evaluar si las células sanguíneas del paciente eran capaces de mantener la actividad también durante un largo tiempo, se midió la longitud telomérica de los leucocitos de la sangre periférica. Los telómeros son estructuras existentes en las puntas de los cromosomas que sirven para proteger al ADN. Siempre que una célula se divide, estas estructuras disminuyen de tamaño, hasta un determinado momento en que la célula ya no logra proliferar y se muere o entra en senescencia. Pero los resultados de la investigación indicaron que los telómeros de los leucocitos analizados eran largos.
“Esto indica que esas células sanguíneas eran capaces de mantener la actividad durante un largo tiempo sin agotarse”, explica Bazzo Catto.
Una de las hipótesis que se plantean en el estudio indica que la existencia de la mutación somática en las células sanguíneas y la recuperación del proceso de renovación celular de la sangre que la misma genera pueden haber hecho su aporte para que el paciente no exhibiera manifestaciones extrahematológicas del síndrome de deficiencia de GATA2, tales como sordera, linfedema y trombosis. De esta forma, la recuperación precoz de la hematopoyesis en pacientes con la enfermedad mediante trasplantes o, en el futuro, con terapia génica, puede ser beneficiosa y evitaría otras complicaciones clínicas, según sugieren los autores del estudio.
“El paciente se aplicó una terapia génica natural. Básicamente, hizo un ensayo experimental que abre la perspectiva ahora de mimetizar este fenómeno en estudios de terapia génica en pacientes con GATA2 a mediano plazo”, sostiene Bazzo Calado.
Amén de su contribución al avance en el tratamiento de la enfermedad y en la asesoría genética de pacientes, este estudio también expande la comprensión de la biología de las células madre hematopoyéticas, afirma el investigador.
“Los resultados de este estudio permiten avanzar en la comprensión de la recuperación de las células madre, componiendo un defecto genético inicial”, remarca Bazzo Calado.
Los suscriptores de la revista Blood pueden leer el artículo intitulado Somatic genetic rescue in hematopoietic cells in GATA2 deficiency (DOI: 10.1182/blood.2020005538), de Luiz Fernando B. Catto, Gustavo Borges, André L. Pinto, Diego V. Clé, Fernando Chahud, Barbara A. Santana, Flavia S. Donaires y Rodrigo T. Calado, en el siguiente enlace: ashpublications.org/blood/article-abstract/136/8/1002/461035/Somatic-genetic-rescue-in-hematopoietic-cells-in?redirectedFrom=fulltext.
Y el editorial intitulado Natural gene therapy in hematopoietic disorders: GATA too, cuya autoría es de Marjolijn C. Jongmans y Roland P. Kuiper, se puede leer en: ashpublications.org/blood/article/136/8/923/463248/Natural-gene-therapy-in-hematopoietic-disorders.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





