
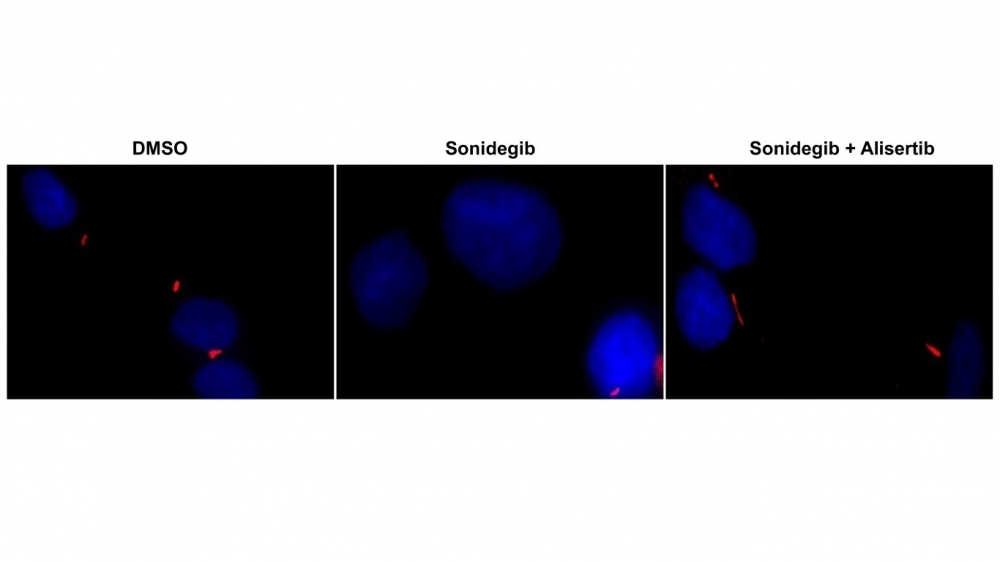
A la izquierda, células tumorales (en azul) con cilios preservados (en rojo); en el medio, tras el tratamiento con sonidegib, se pierden los cilios; a la derecha, los cilios se recuperan luego de la combinación de sonidegib con alisertib (imagen: Taciani Magalhães)
El tipo de ependimoma estudiado afecta principalmente a los niños, posee una baja tasa de sobrevida y no existe para él un tratamiento quimioterapéutico específico. La combinación de dos fármacos experimentales inhibió el crecimiento tumoral in vitro
El tipo de ependimoma estudiado afecta principalmente a los niños, posee una baja tasa de sobrevida y no existe para él un tratamiento quimioterapéutico específico. La combinación de dos fármacos experimentales inhibió el crecimiento tumoral in vitro

A la izquierda, células tumorales (en azul) con cilios preservados (en rojo); en el medio, tras el tratamiento con sonidegib, se pierden los cilios; a la derecha, los cilios se recuperan luego de la combinación de sonidegib con alisertib (imagen: Taciani Magalhães)
Por André Julião | Agência FAPESP – Un estudio a cargo de científicos de Brasil, Australia, Austria y Estados Unidos ha avanzado en la comprensión de un tipo de cáncer pediátrico sin opciones de tratamiento farmacológico y con baja tasa de sobrevivencia. Los resultados, publicados en la revista Neuro-Oncology, abren el camino hacia la búsqueda de terapias más específicas.
“Los denominados ependimomas son tumores del sistema nervioso central bastante heterogéneos y sin muchas opciones de tratamiento, más allá de la cirugía y la radioterapia. Nuestro estudio se enfocó en el llamado ependimoma supratentorial con fusión de los genes C11orf95 y RELA [ST-RELA, por sus siglas en inglés], un subgrupo frecuente en la población pediátrica que es agresivo, de mal pronóstico y carente de un tratamiento específico”, informa Taciani de Almeida Magalhães, primera autora del estudio, realizado durante su doctorado en la Facultad de Medicina de Ribeirão Preto, de la Universidad de São Paulo (FMRP-USP), en Brasil, con el apoyo de la FAPESP.
Este trabajo forma parte de un Proyecto Temático coordinado por Luiz Gonzaga Tone, docente de la FMRP-USP, quien dirigió la referida investigación doctoral y es uno de los coautores del artículo.
Este tipo de ependimoma afecta fundamentalmente a niños con edades alrededor de los 8 años al momento del diagnóstico. La tasa de sobrevida cinco años después del tratamiento es de aproximadamente el 30 %, particularmente entre los pacientes en quienes la extirpación total del tumor mediante cirugía no es posible.
No existen medicamentos específicos y, por ende, la única opción terapéutica disponible aparte de la cirugía en estos casos es la radioterapia, que puede causar serias secuelas cognitivas y motoras en los niños.
Con la ayuda de diferentes técnicas, los investigadores descubrieron que en estos tumores la denominada vía de señalización celular Hedgehog (Hh) se encuentra bastante activa. Por eso los trataron en laboratorio con sonidegib, un medicamento que inhibe la vía Hh y que actualmente pasa por ensayos clínicos para otros tumores del sistema nervioso central.
Con todo, al examinar los tumores tratados, los investigadores observaron que habían perdido determinadas estructuras conocidas como cilios primarios y, como consecuencia de ello, se volvieron resistentes al fármaco. Se hacía entonces necesario recuperar los cilios.
Al regresar a los bancos del laboratorio, el grupo constató que la formación de los cilios estaba regulada por una proteína específica llamada AURKA. No por casualidad, esta se encuentra presente en otros tumores, por eso se contaba también con un inhibidor específico en ensayos clínicos, el alisertib.
Aparte del sonidegib, los investigadores empezaron entonces a tratar los tumores con alisertib. Los cilios primarios no se perdieron y el sonidegib pudo así actuar exitosamente provocando la muerte de las células tumorales, sin afectar a las sanas.
Como la combinación de fármacos funcionaba en el modelo in vitro, los investigadores pasaron a efectuar pruebas en animales, en el marco de una colaboración con un grupo de Australia. Trataron ratones que desarrollaron tumores cerebrales con esta combinación. No obstante, para asombro de los investigadores, no se verificó ninguna extensión de la sobrevida en los animales en comparación con los ratones de control, a los que no se les aplicó el tratamiento.
El grupo de científicos estima que la capa que recubre los vasos sanguíneos del cerebro para protegerlos del medio externo, la denominada barrera hematoencefálica, impide que el medicamento llegue a los tumores.
“Otros estudios han demostrado que los inhibidores de la proteína AURKA, la que promueve la pérdida de los cilios primarios, no llegaron al cerebro. Esta es una posible explicación del hecho de que nuestro tratamiento no haya funcionado en animales”, explica De Almeida Magalhães, quien actualmente lleva adelante una pasantía posdoctoral en la Harvard Medical School, en Estados Unidos. Anteriormente, la investigadora había concretado parte de su doctorado en esa misma institución con beca de la FAPESP.
Las alternativas
Ahora, los investigadores buscan otros medicamentos con idéntica acción que logren atravesar la barrera hematoencefálica y así quizá llegar finalmente más cerca de un tratamiento inédito contra estos tumores.
“Aun cuando la combinación no ha tenido el éxito esperado en el modelo animal, ahora conocemos los mecanismos moleculares de los tumores y, por ende, surge así un camino que ha de seguirse y que no se conocía”, afirma la investigadora.
Para Elvis Terci Valera, profesor colaborador del Posgrado del Programa de Salud Infantil y Adolescente de la FMRP-USP, quien también colaboró con el estudio, este descubrimiento abre perspectivas rumbo a la concreción de estudios clínicos con generaciones más modernas de fármacos inhibidores de la vía Hh y de la proteína AURKA con una mejor penetración en el sistema nervioso central.
“Otra estrategia consistiría en aplicar estos medicamentos más modernos directamente en el líquido cefalorraquídeo que circula en el cerebro y en la médula espinal. Podrían estudiarse opciones como esta, a los efectos de revertir la resistencia al tratamiento”, culmina Terci Valera.
Puede leerse el estudio intitulado Activation of Hedgehog signaling by the oncogenic RELA fusion reveals a primary cilia-dependent vulnerability in supratentorial ependymoma en el siguiente enlace: academic.oup.com/neuro-oncology/advance-article-abstract/doi/10.1093/neuonc/noac147/6596001.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.




