

Investigadores del país develaron los mecanismos que hacen que la cepa brasileña de la bacteria E. coli productora de la toxina Shiga –que contamina a los alimentos– sea menos virulenta y patogénica que las de otros lugares. Estos resultados pueden ser útiles para delinear estrategias de monitoreo epidemiológico (Células epiteliales humanas infectadas con la STEC. Las manchas corresponden a la toxina Shiga; imagen: S. Schuller/ Wellcome Collection)
Investigadores del país develaron los mecanismos que hacen que la cepa brasileña de la bacteria E. coli productora de la toxina Shiga –que contamina a los alimentos– sea menos virulenta y patogénica que las de otros lugares. Estos resultados pueden ser útiles para delinear estrategias de monitoreo epidemiológico
Investigadores del país develaron los mecanismos que hacen que la cepa brasileña de la bacteria E. coli productora de la toxina Shiga –que contamina a los alimentos– sea menos virulenta y patogénica que las de otros lugares. Estos resultados pueden ser útiles para delinear estrategias de monitoreo epidemiológico
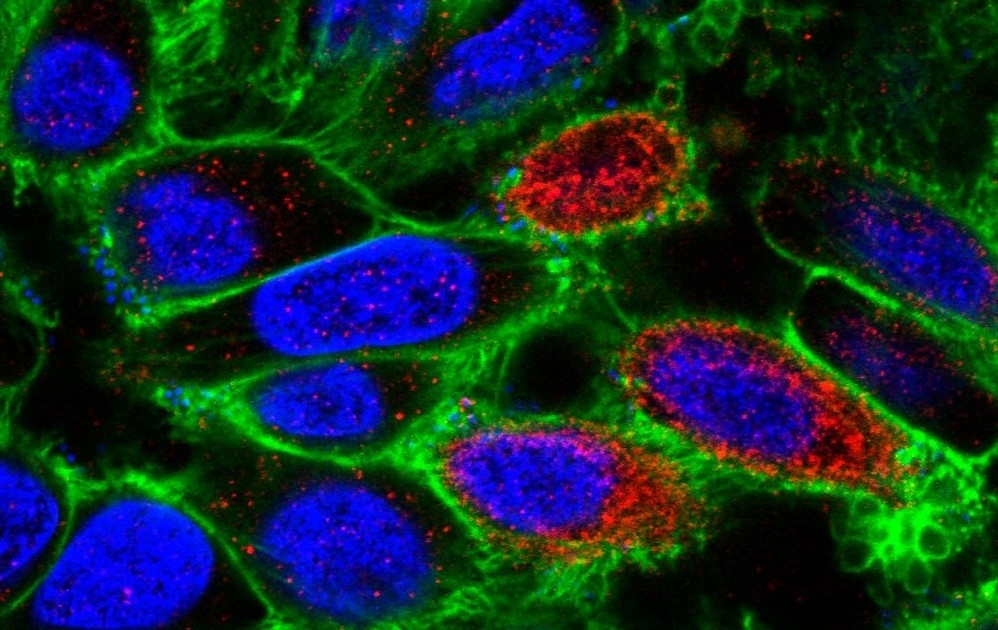
Investigadores del país develaron los mecanismos que hacen que la cepa brasileña de la bacteria E. coli productora de la toxina Shiga –que contamina a los alimentos– sea menos virulenta y patogénica que las de otros lugares. Estos resultados pueden ser útiles para delinear estrategias de monitoreo epidemiológico (Células epiteliales humanas infectadas con la STEC. Las manchas corresponden a la toxina Shiga; imagen: S. Schuller/ Wellcome Collection)
Por Elton Alisson | Agência FAPESP – Entre las bacterias de la especie Escherichia coli, habitantes comunes del tracto digestivo humano, existe un grupo capaz de producir una toxina llamada Shiga que ha venido intrigando los microbiólogos.
En países tales como Australia, Estados Unidos, Japón y Argentina, el consumo de carne vacuna infectada con cepas de esta bacteria, conocida como STEC (las siglas en inglés de E. coli productora de toxina Shiga), ha venido siendo asociado al desarrollo de una enfermedad grave denominada síndrome hemolítico urémico (SHU), que causa insuficiencia renal y que acomete principalmente a niños con menos de cinco años. En Brasil, por otra parte, un determinado serotipo de STEC se ha hallado en la carne y en los excrementos de animales vacunos −reservorios naturales de estas bacterias−, pero nunca en pacientes diagnosticados con SHU.
En el marco de un estudio realizado en colaboración con investigadores del Instituto Butantan y de la Universidad Federal de São Paulo (Unifesp), científicos de la Universidad de São Paulo (USP), en Brasil, han develado ahora algunos mecanismos moleculares que vuelven a la STEC “extranjera” más virulenta y más patogénica que la cepa brasileña.
Estos descubrimientos, realizados en el marco de un proyecto que contó con el apoyo de la FAPESP, se publicaron como destacados de portada en la revista Microorganisms.
“Los resultados de este estudio pueden ayudar a identificar nuevos marcadores moleculares de virulencia y patogenicidad para bacterias STEC, que resultarán útiles a los efectos de delinear estrategias de monitoreo epidemiológico. El riesgo reside en que la cepa brasileña sufra alguna modificación genética que la vuelva capaz de causar también la enfermedad”, declaró a Agência FAPESP Carlos Alberto Moreira Filho, docente del Departamento de Pediatría de la Facultad de Medicina de la USP (FM-USP) y coordinador del proyecto.
De acuerdo con Moreira Filho, la STEC causante del SHU perdura durante más tiempo en el intestino y libera paulatinamente la Shiga. Esta toxina atraviesa la barrera intestinal, entra en el torrente sanguíneo y llega a los riñones, donde provoca lesiones y, por ende, la insuficiencia de estos órganos.
A los efectos de entender la diferencia entre este microorganismo y las cepas que no provocan la enfermedad, los investigadores realizaron un estudio que salió publicado en 2017 en la revista PLOS ONE, en el cual compararon el genoma de una cepa aislada en un paciente australiano diagnosticado con SHU, denominada EH41, y el de una cepa brasileña aislada en excrementos bovinos, la Ec472/01.
Los resultados indicaron que en la EH41 se expresan 15 genes, entre ellos el regulador de virulencia dicA, que no se encuentran activos en la cepa brasileña.
“Con este estudio logramos dilucidar la diferencia genética y genómica entre la cepa australiana y la brasileña”, dijo Moreira Filho.
Para analizar la respuesta de las células de la capa superficial del intestino delgado a ambas cepas, los investigadores efectuaron entonces un experimento con células humanas del linaje Caco-2 cultivadas en laboratorio.
“Ese linaje de células mimetiza muy bien la capa de células epiteliales [enterocitos] del intestino delgado, a la cual las bacterias STEC se adhieren para crear colonias”, explicó Moreira Filho.
Las bacterias EH41 y la Ec472/01 quedaron dispuestas sobre esas células durante tres horas. Mediante un abordaje de biología de sistemas, se analizaron las alteraciones en los patrones globales de expresión génica de los cultivos en el transcurso de las tres horas, a intervalos secuenciales de 7,5 minutos.
En tanto, mediante microscopía electrónica de barrido, se evaluaron las alteraciones morfológicas en las células Caco-2 a intervalos de una, dos y tres horas.
Los resultados de los análisis indicaron que la cepa asociada a la SHU expresa un conjunto de genes de virulencia que induce una respuesta distinta de los enterocitos humanos, y esto puede estar relacionado con su mayor patogenicidad.
La activación de estos genes hace que la cepa causante de SHU les impida a los enterocitos expresar determinadas reacciones de defensa, y así permite que el patógeno permanezca durante más tiempo en el intestino. De este modo, produce lentamente la toxina Shiga, que ingresa en el torrente sanguíneo y llega a los riñones.
Los enterocitos, que también son células de inmunidad natural, fallan en su misión de detener a la bacteria y permiten que esta persista en el tejido y libere la toxina Shiga”, dijo Moreira Filho.
El análisis de redes
Para analizar la expresión y también la interacción de los genes de los enterocitos en el transcurso del tiempo inducida por la exposición a las cepas de las bacterias, se aplicó una metodología de visualización en 3D de redes de coexpresión génica, mediante el empleo de un software desarrollado por investigadores del Instituto de Física de São Carlos (IFSC) de la USP. También se aplicaron modelos matemáticos desarrollados por el grupo del profesor Roberto Marcondes César Junior, del Instituto de Matemática y Estadística (IME) de la USP, en el marco de un proyecto que contó con el apoyo de la FAPESP.
Estos modelos matemáticos permiten detectar variaciones en la topología de una red, alteraciones en el nivel jerárquico que los genes ejercen en una red en términos de influencia sobre la expresión de los restantes.
“Los algoritmos se enfocan en los genes en funcionamiento y montan redes. Esto permite detectar agrupamientos o módulos que explican por qué determinados genes están conectados en una situación y no en otras. Y hace posible incluso simular qué generaría la inactivación de un determinado gen en una red”, dijo César Junior.
Los análisis mostraron que la bacteria asociada a la SHU causa una variación abrupta de la topología de las redes de coexpresión génica de las células Caco-2 en el transcurso de las tres horas de interacción.
“La bacteria causa una pérdida de conectividad entre los genes de las células, que quedan así con menos conexiones”, dijo Moreira Filho.
En tanto, el análisis de los grupos de genes mostró que la bacteria causante de la enfermedad induce la inflamación y la muerte de la célula Caco-2 desde la primera hora de exposición, mientras que la cepa brasileña provocó menos alteraciones genéticas, fundamentalmente en la estructura de las células (el citoesqueleto) y una respuesta inmune moderada.
A su vez, la microscopía electrónica reveló que EH41, en comparación con Ec472/01, causa en las células Caco-2 una destrucción mucho más intensa de las microvellosidades, que son estructuras típicas de enterocitos sanos.
“Estas constataciones ayudan a entender los mecanismos de inducción de la respuesta inmune que pueden derivar en condiciones graves como el SHU”, dijo Moreira Filho.
A juicio del investigador, este estudio indica la necesidad de realizar nuevos estudios sobre la influencia de los factores ambientales en la virulencia de las STEC, incluso acerca de su paso por el tracto digestivo de vacunos y humanos.
“Debemos entender si el paso de esta bacteria por el sistema digestivo del ganado brasileño, que tiene una alimentación distinta, altera la expresión y desconecta esos genes de virulencia, por ejemplo”, afirmó.
Puede leerse el estudio intitulado Dynamic gene network analysis of Caco-2 cell response to Shiga toxin-producing Escherichia coli-associated hemolytic-uremic syndrome (DOI: 10.3390/microorganisms7070195), de Silvia Y. Bando, Priscila Iamashita, Filipi N. Silva, Luciano da F. Costa, Cecilia M. Abe, Fernanda B. Bertonha, Beatriz E. C. Guth, André Fujita y Carlos A. Moreira-Filho, en la revista Microorganisms, en el siguiente enlace: www.mdpi.com/2076-2607/7/7/195.
Y puede accederse al artículo A hemolytic-uremic syndrome-associated strain O113:H21.Shiga toxin-producing Escherichia coli specifically expresses a transcriptional module containing dicA and is related to gene network dysregulation in Caco-2 cells (DOI: 10.1371/journal.pone.0189613), de Silvia Yumi Bando, Priscila Iamashita, Beatriz E. Guth, Luis F. dos Santos, André Fujita, Cecilia M. Abe, Leandro R. Ferreira y Carlos Alberto Moreira-Filho, ingresando a la revista PLOS ONE en el siguiente vínculo: journals.plos.org/plosone/article?id=10.1371/journal.pone.0189613.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





