

Pesquisadores do CEPID CRID descobrem que medicamento amplamente utilizado tem efeito alternativo capaz de ativar o receptor celular da resposta imune inata. Achado amplia estratégias de tratamento contra o câncer (ilustração: CRID)
Pesquisadores do CEPID CRID descobrem que medicamento amplamente utilizado tem efeito alternativo capaz de ativar o receptor celular da resposta imune inata. Achado amplia estratégias de tratamento contra o câncer
Pesquisadores do CEPID CRID descobrem que medicamento amplamente utilizado tem efeito alternativo capaz de ativar o receptor celular da resposta imune inata. Achado amplia estratégias de tratamento contra o câncer
Pesquisadores do CEPID CRID descobrem que medicamento amplamente utilizado tem efeito alternativo capaz de ativar o receptor celular da resposta imune inata. Achado amplia estratégias de tratamento contra o câncer (ilustração: CRID)
Maria Fernanda Ziegler | Agência FAPESP – Pesquisadores descobriram um novo efeito para um medicamento quimioterápico amplamente utilizado e oferecido a pacientes do Sistema Único de Saúde (SUS).
O paclitaxel é indicado em casos de câncer de mama, câncer de pulmão, ovário e outros tipos de tumores. Além de ser um antineoplásico, ou seja, inibir o desenvolvimento do tumor (ao interromper o ciclo celular), o novo estudo indica que o medicamento também é capaz de reativar a resposta imune, combatendo assim o tumor em duas frentes.
Em artigo, publicado na revista Cancer Research, cientistas do Centro de Pesquisa em Doenças Inflamatórias (CRID) – um Centro de Pesquisa, Inovação e Difusão (CEPID) financiado pela FAPESP – e da Universidade Federal do Ceará (UFC) descrevem como o medicamento reativa a resposta imune inata.
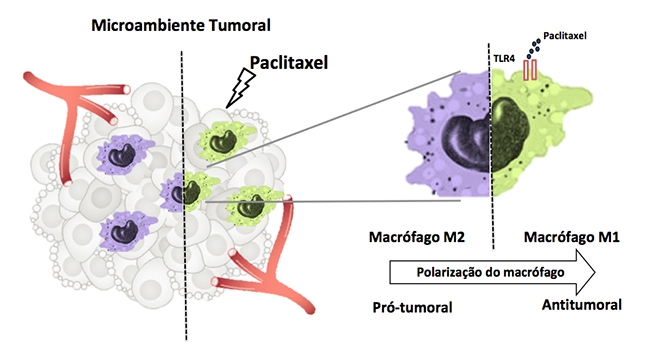
Estudos anteriores apontaram que o paclitaxel teria um efeito alternativo de estimular o sistema imunológico de roedores. Também é conhecido que macrófagos (células de defesa do sistema imune) apresentam dois fenótipos: um com ação pró-inflamatória e antitumoral (M1) e, outro, com propriedade anti-inflamatória que atua como um estimulador do crescimento do tumor (M2).
Na nova pesquisa, os autores uniram esses dois conceitos e descobriram que a ação alternativa do paclitaxel serve como um modulador da resposta imune e que, a partir do receptor TLR4, reprograma o macrófago para o fenótipo antitumoral M1.
“Reunimos esses dois conceitos e descobrimos o efeito alternativo do quimioterápico. Identificar que o paclitaxel modula a resposta imune abre uma nova perspectiva de uso do medicamento”, disse Carlos Wagner Wanderley, primeiro autor do artigo, à Agência FAPESP.
Se confirmada em testes clínicos, a descoberta possibilita associar o paclitaxel a tratamentos mais modernos contra o câncer, como é o caso da imunoterapia, estratégia de tratamento que estimula o sistema imune do paciente a combater o tumor.
“Essa associação pode atacar o tumor em três frentes: o paclitaxel pode induzir parada da mitose nas células neoplásicas e ativação de macrófagos, enquanto a imunoterapia pode estimular a ação antitumoral dos linfócitos”, disse Wanderley.
A descoberta é resultado do doutorado de Wanderley, da UFC, que realizou o estudo em parceria com pesquisadores do CRID nos laboratórios do centro, em Ribeirão Preto (SP).
“O estudo começou com uma ideia simples, sabia-se que o paclitaxel tinha entre seus efeitos colaterais a dor neuropática, ligada ao receptor TLR4, e agora acreditamos que essa descoberta tenha um impacto grande na clínica também”, disse Thiago Mattar Cunha, professor associado da Faculdade de Medicina de Ribeirão Preto e um dos autores do estudo.
Mattar Cunha explica que o estudo envolveu experimentos em cultura celular, modelo animal e análises de bioinformática. Primeiro, para demonstrar a atuação do medicamento na resposta imune inata, transformaram macrófagos in vitro em estágio inativo (repouso, chamado M0) para um padrão anti-inflamatório e pró-tumoral chamado M2. Ao aplicar paclitaxel, os macrófagos M2 foram reprogramados para o perfil M1 (antitumoral).
Depois do estudo em cultura celular, o grupo passou a fazer os experimentos in vivo em camundongos transgênicos deficientes em receptor TLR4 nos macrófagos.
“Nesses casos, vimos que o quimioterápico perdeu o seu efeito. Usamos uma linhagem tumoral resistente ao paclitaxel e a seu efeito antiproliferativo. Observamos que, mesmo sem a ação antiproliferativa, o medicamento continuava modulando o sistema imunológico”, disse Mattar Cunha.
Melhor resposta
Os pesquisadores, além dos experimentos in vitro e in vivo, fizeram também análises de bioinformática a partir de um banco de dados de expressão gênica de amostras de tumores de pacientes com câncer de ovário que receberam o tratamento com o paclitaxel.
“Ao analisar as biópsias, foi possível identificar um perfil de genes característicos de macrófagos com perfil M1 (antitumoral) nos tumores tratados com o quimioterápico, o que condiz com a nossa hipótese”, disse Mattar Cunha.
Os pesquisadores querem avançar nos estudos e fazer testes clínicos com o quimioterápico.
“Vamos trabalhar em duas linhas: estudar outros medicamentos quimioterápicos mais antigos para ver se eles também têm ação imune antitumoral e fazer testes clínicos com o paclitaxel. No CRID, trabalhamos com assessores internacionais, que demostraram interesse em fazer pesquisa clínica para saber se o medicamento funciona como um adjuvante nas terapias”, disse Fernando Queiroz Cunha, coordenador do CRID.
Queiroz Cunha explica que a associação mais interessante seria com as chamadas checkpoints therapies, imunoterapia que bloqueia proteínas que impedem o sistema imunológico de atacar as células cancerígenas.
“É uma terapia que tenta melhorar a resposta imune e o efeito do paclitaxel é exatamente isso. Talvez ele possa ser usado como terapia adjuvante para outros tumores”, disse.
A descoberta pode ter ainda efeito importante no custo dos tratamentos. “Estima-se que o custo total do tratamento com inibidores de checkpoint pode atingir hoje R$ 1 milhão por paciente. Já o custo dessas drogas mais antigas como o paclitaxel, que entrou no mercado no início dos anos 1990, é muito mais baixo. Com base na descoberta, é possível propor a combinação de fármacos em busca de algo a mais do que o previsto no passado”, disse Roberto Lima-Junior, professor do departamento de Fisiologia e Farmacologia da UFC, que também participou da pesquisa.
O artigo Paclitaxel reduces tumor growth by reprogramming tumor-associated macrophages to an M1- profile in a TLR4-dependent manner (doi: 10.1158/0008-5472.CAN-17-3480), de Carlos W. Wanderley, David F. Colon, Joao Paulo Mesquita Luiz, Francisco F. Oliveira, Paula R. Viacava, Caio A. Leite, Janaina A. Pereira, Camila M. Silva, Cassia R. Silva, Rangel L. Silva, Cesar A. Speck-Hernandez, Jose M. Mota, Jose C. Alves-Filho, Roberto C. Lima-Júnior, Thiago M. Cunha e Fernando Q. Cunha, pode ser lido em http://cancerres.aacrjournals.org/content/early/2018/08/11/0008-5472.CAN-17-3480.
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





