

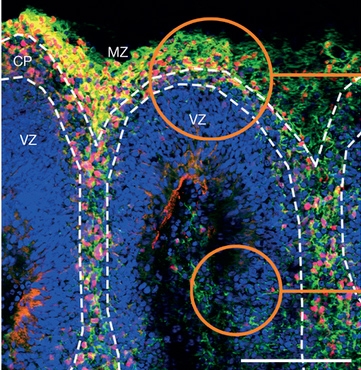
Experimentos com camundongos descritos na Nature confirmam que o ZIKV atravessa a barreira placentária, infecta e mata as células do cérebro em formação. Dados in vitro indicam que linhagem brasileira é mais agressiva que a original africana (imagem representativa dos organoides cerebrais humanos, mostrando a zona marginal (MZ), a placa cortical (CP) e a zona ventricular)
Experimentos com camundongos descritos na Nature confirmam que o ZIKV atravessa a barreira placentária, infecta e mata as células do cérebro. Dados in vitro indicam que linhagem brasileira é mais agressiva
Experimentos com camundongos descritos na Nature confirmam que o ZIKV atravessa a barreira placentária, infecta e mata as células do cérebro. Dados in vitro indicam que linhagem brasileira é mais agressiva

Experimentos com camundongos descritos na Nature confirmam que o ZIKV atravessa a barreira placentária, infecta e mata as células do cérebro em formação. Dados in vitro indicam que linhagem brasileira é mais agressiva que a original africana (imagem representativa dos organoides cerebrais humanos, mostrando a zona marginal (MZ), a placa cortical (CP) e a zona ventricular)
Karina Toledo | Agência FAPESP – Um estudo conduzido no âmbito da Rede Zika, apoiada pela FAPESP, e divulgado nesta quarta-feira (11/05) na revista Nature apresentou a evidência definitiva de que a infecção pelo vírus Zika (ZIKV) durante a gestação pode causar má-formação cerebral congênita, confirmando que a doença está relacionada ao surto de microcefalia registrado no Brasil em 2015.
Por meio de experimentos com camundongos, o grupo da Universidade de São Paulo (USP) mostrou que o ZIKV é capaz de atravessar a barreira placentária, infectar e matar as células que dariam origem ao cérebro dos animais em gestação.
Dados de testes in vitro sugerem ainda que a linhagem brasileira do vírus é mais agressiva do que a linhagem africana, que originalmente infectava macacos. Isso corrobora a teoria de que, nos últimos anos, o ZIKV teria sofrido mutações que o tornaram mais eficiente para infectar humanos (leia mais em http://agencia.fapesp.br/22345).
“Não há mais dúvidas de que o vírus Zika é neurotóxico e pode causar microcefalia. A lesão que encontramos nos cérebros dos filhotes, caracterizada principalmente pela redução da espessura do córtex [camada mais externa e sofisticada do cérebro dos vertebrados], é muito característica e também foi vista nos bebês humanos. Além disso, encontramos o vírus se replicando no cérebro dos camundongos recém-nascidos em quantidades muito maiores do que em outros órgãos”, comentou Jean Pierre Peron, professor do Instituto de Ciências Biomédicas (ICB) da USP e um dos autores do artigo.
Parte das conclusões está baseada em experimentos feitos com camundongos da linhagem SJL que, segundo Peron, mostraram-se bom modelo para o estudo da doença. As fêmeas foram infectadas entre o 10º e o 12º dia de gestação com uma linhagem viral isolada de um bebê nascido com microcefalia na Paraíba, em 2015.
Imediatamente após o parto, foi possível notar uma redução no crescimento global dos filhotes expostos ao ZIKV. Enquanto o peso médio ao nascer das crias de fêmeas controle (não infectadas) era 3,4 gramas, a média dos filhotes infectados era 1,4 grama. Medidas do crânio – comprimento e altura – apresentaram diminuição de pelo menos um terço no grupo exposto ao ZIKV.
Análises do tecido cerebral feitas ao microscópio mostraram redução da camada cortical, bem como alteração no número e na morfologia das células dessa região, como explicou Patricia Beltrão-Braga, pesquisadora da Faculdade de Medicina Veterinária e Zootecnia (FMVZ) da USP.
“As análises histológicas revelaram um fenótipo celular atípico, principalmente no córtex, mas também no hipotálamo e no tálamo. As células apresentaram o que chamamos de núcleo vacuolado, ou seja, a cromatina estava toda espremida em um canto do núcleo, que à primeira vista parecia estar vazio”, contou Beltrão-Braga.
Segundo os pesquisadores, esse fenótipo costuma ser observado durante processos que levam à morte celular. De fato, análises de expressão gênica feitas posteriormente revelaram que, nos filhotes expostos ao ZIKV, genes associados a processos de apoptose (morte celular programada) e autofagia (no qual a célula degrada e reabsorve suas estruturas internas) estavam superexpressos em comparação ao grupo controle.
Para complementar os ensaios in vivo, foram realizados nos diversos tecidos dos camundongos recém-nascidos testes moleculares do tipo de PCR (reação em cadeia da polimerase) em tempo real, capazes de detectar o RNA viral durante a fase aguda da infecção.
“Encontramos o vírus se replicando no baço, no fígado e no rim, mas em quantidades muito menores do que as observadas no cérebro”, disse Peron.
“O conjunto de resultados mostra que o vírus tem enorme preferência pelas células do sistema nervoso. Não apenas detectamos no cérebro maior quantidade de RNA viral como também os principais efeitos da infecção”, acrescentou Beltrão-Braga.
Curiosamente, os mesmos achados não foram observados nos primeiros testes feitos na USP com camundongos da linhagem C57BL/6, os mais usados em laboratórios.
“Essa linhagem tem, sabidamente, uma resposta imunológica mais robusta, com maior produção de citocinas do tipo interferon alfa e beta. Acreditamos que isso tenha possibilitado aos animais eliminar o vírus do organismo de forma mais eficaz, impedindo sua passagem pela barreira placentária. Testamos com diferentes doses do vírus e diferentes datas de infecção e, em nenhum caso, os filhotes nasceram com qualquer tipo de má-formação”, contou Peron.
Para o pesquisador, esse fato evidencia a influência da genética materna na extensão do dano causado pelo vírus ao feto. “Assim como ocorre com camundongos, certamente deve haver mães humanas mais suscetíveis ao vírus e outras mais resistentes. Os mecanismos envolvidos ainda precisam ser estudados”, ponderou.
Minicérebros
Nos testes in vitro foram usados três diferentes modelos desenvolvidos a partir de células humanas: culturas bidimensionais (em placa de vidro) de neurônios e de células progenitoras neurais (um tipo de célula-tronco capaz de se diferenciar em neurônios e células da glia); culturas tridimensionais de células progenitoras neurais (cultivadas em suspensão para formar as chamadas neuroesferas); e organoides cerebrais ou minicérebros (estruturas tridimensionais milimétricas criadas em laboratório a partir de células-tronco pluripotentes induzidas e capazes de mimetizar o cérebro de fetos no primeiro trimestre de gestação).
Nos três modelos foi comparado o efeito da exposição à linhagem brasileira de ZIKV, à linhagem africana e também ao vírus da febre amarela.
“Decidimos usar o vírus da febre amarela, que também é da família Flaviviridae como o Zika e a dengue, como uma espécie de controle negativo. Para ter certeza de que os efeitos observados não seriam resultantes de qualquer infecção viral, mas específicos do Zika”, explicou Beltrão-Braga.
No experimento feito com as culturas bidimensionais, o grupo observou que os três vírus foram capazes de infectar tanto os neurônios quanto as células progenitoras neurais, sendo que não houve morte celular apenas na cultura exposta ao vírus da febre amarela. Ao comparar as duas culturas infectadas com ZIKV, notou-se que as células progenitoras neurais morreram bem mais do que os neurônios.
Segundo Peron, uma das possíveis explicações para a maior suscetibilidade das células progenitoras neurais pode ser o fato de elas expressarem em maior quantidade uma família de receptores de membrana conhecida como TAM. Estudos anteriores indicaram que esses receptores – chamados Tyro3, AXL e MertK – facilitam a entrada do vírus da dengue e do Zika nas células humanas.
Nos testes feitos com as neuroesferas, formadas apenas pelas células progenitoras, foi possível perceber claramente ao microscópio o dano causado pelo ZIKV, principalmente a linhagem brasileira.
Enquanto as neuroesferas controle (não infectadas) dobraram de tamanho num período de quatro dias, as infectadas pela linhagem africana cresceram, mas muito pouco, mostrando que houve morte celular. Já as neuroesferas infectadas pelo vírus brasileiro foram reduzidas a menos de um terço do tamanho inicial e apresentaram uma estrutura desorganizada, que evidencia a ativação de processos de morte celular.
Observou-se ainda que, quanto maior era a quantidade de vírus no meio, maior era a destruição celular. Para Beltrão-Braga, isso pode explicar a ocorrência de má-formações com diferentes graus de severidade entre os bebês que nasceram com microcefalia no Brasil.
Finalmente, com os minicérebros infectados com a linhagem brasileira, observou-se que as mortes se concentraram nas áreas onde estava ocorrendo maior neurogênese (produção de novos neurônios), sendo que alguns subtipos celulares foram praticamente exterminados após quatro dias.
Já os organoides com o vírus africano não apresentaram diferença significativa em relação aos minicérebros expostos ao vírus de febre amarela. Nas áreas já diferenciadas, como a que daria origem ao córtex, neurônios e células progenitoras neurais morreram tanto no caso do vírus brasileiro quanto do africano.
Para complementar as análises in vitro, os pesquisadores compararam a infecção pela linhagem brasileira do ZIKV em minicérebros humanos e em organoides construídos a partir de células pluripotentes de chimpanzé.
“Os resultados mostram que a linhagem brasileira está tão diferente da original africana que já não é capaz de infectar os organoides de chimpanzé, embora a similaridade entre o genoma humano e o desses primatas seja de 99%. Aparentemente, o ZIKV sofreu ao longo dos últimos anos mutações que o tornaram mais ‘humanizado’ e capaz de causar as má-formações que estamos vendo nos recém-nascidos brasileiros”, avaliou Beltrão-Braga.
Desdobramentos
Na avaliação de Peron, ao mostrar que camundongos da linhagem SJL são um bom modelo para o estudo da infecção pelo ZIKV, o artigo abre caminho para pesquisas voltadas ao desenvolvimento de vacinas e de métodos para proteger fetos de mães infectadas.
“Em meu laboratório, o principal interesse no momento é entender a biologia por trás dessa interação do vírus com os receptores TAM e por que isso causa a morte massiva das células progenitoras neurais. Queremos entender quais vias são ativadas pela interação do vírus com esses receptores”, disse o pesquisador do ICB-USP.
Além de tentar entender por que os neurônios são menos afetados que as células progenitoras, Beltrão-Braga também está interessada em descobrir formas de evitar a morte celular induzida pelo vírus. “Precisamos desvendar qual é o tipo de resposta imunológica desencadeada no cérebro e se ela favorece ou minimiza a morte das células”, afirmou.
O artigo publicado na Nature contou com a colaboração do coordenador da Rede Zika, Paolo Zanotto (ICB-USP), e de Alysson Muotri, pesquisador na Universidade da Califórnia em San Diego, nos Estados Unidos. As análises foram conduzidas principalmente pelas pós-graduandas da FMVZ-USP Fernanda Cuogola, Isabella Fernandes e Fabiele Russo.
O artigo The Brazilian Zika virus strain causes birth defects in experimental models (doi:10.1038/nature18296), de Fernanda R. Cugola e outros, publicado na Nature, pode ser lido em www.nature.com/nature/journal/vnfv/ncurrent/full/nature18296.html.
Vídeos com pesquisadores da USP que participaram do estudo podem ser assistidos em: www.youtube.com/playlist?list=PLwA0zWYFcS_g1FxdtBz5OyaiIqdaLpbQv
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





