

Un estudio del Centro de Investigación en Enfermedades Inflamatorias indica que este medicamento oncológico es capaz de reactivar el sistema imunológico, y abre posibilidades de nuevas estrategias de tratamiento (ilustración: CRID)
Un estudio del Centro de Investigación en Enfermedades Inflamatorias indica que este medicamento oncológico es capaz de reactivar el sistema imunológico, y abre posibilidades de nuevas estrategias de tratamiento
Un estudio del Centro de Investigación en Enfermedades Inflamatorias indica que este medicamento oncológico es capaz de reactivar el sistema imunológico, y abre posibilidades de nuevas estrategias de tratamiento
Un estudio del Centro de Investigación en Enfermedades Inflamatorias indica que este medicamento oncológico es capaz de reactivar el sistema imunológico, y abre posibilidades de nuevas estrategias de tratamiento (ilustración: CRID)
Por Maria Fernanda Ziegler | Agência FAPESP – Científicos brasileños descubrieron un nuevo efecto de un medicamento quimioterapéutico de amplia utilización y que se aplica con pacientes del Sistema Único de Salud, el SUS, tal como se la conoce a la red de salud pública del país.
El paclitaxel se emplea en casos de cáncer de mama, de pulmón, de ovarios y otros tipos de tumores. Además de ser antineoplásico, es decir, de inhibir el desarrollo de tumores (al interrumpir el ciclo celular), este nuevo estudio indica que este medicamento es también capaz de reactivar la respuesta inmunitaria; por ende, sirve en el combate contra los tumores en dos frentes.
En un artículo publicado en la revista Cancer Research, científicos del Centro de Investigación en Enfermedades Inflamatorias (CRID) –un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la FAPESP– y de la Universidad Federal de Ceará (UFC), en Brasil, describen de qué manera este medicamento reactiva la respuesta inmunitaria innata.
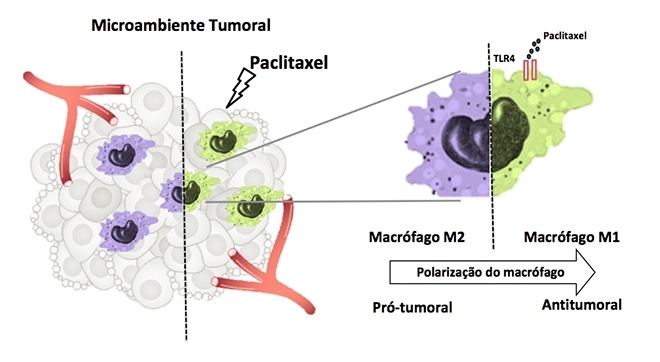
Estudios anteriores indicaron que el paclitaxel tendría un efecto alternativo de estímulo del sistema inmunológico en roedores. También se sabe que los macrófagos (células de defensa del sistema inmunológico) exhiben dos fenotipos: uno con acción proinflamatoria y antitumoral (M1) y el otro con propiedades antiinflamatorias, y que actúa como un estimulador del crecimiento de los tumores (M2).
En esta nueva investigación, los autores unieron estos dos conceptos y descubrieron que la acción alternativa del paclitaxel sirve como moduladora de la respuesta inmunitaria, y que desde el receptor TLR4 reprograma los macrófagos para el fenotipo antitumoral M1.
“Reunimos ambos conceptos y descubrimos el efecto alternativo de este quimioterapéutico. El descubrimiento de que el paclitaxel modula la respuesta inmunitaria abre una nueva perspectiva de uso de este medicamento”, declaró Carlos Wagner Wanderley, primer autor del artículo, a Agência FAPESP.
De confirmarse este descubrimiento en ensayos clínicos, se podrá asociar el paclitaxel con tratamientos más modernos contra el cáncer, como en el caso de la inmunoterapia, una estrategia de tratamiento que estimula al sistema inmunológico del paciente a combatir los tumores.
“Con esta asociación se puede atacar a los tumores en tres frentes: el paclitaxel puede inducir la detención de la mitosis en las células neoplásicas y la activación de los macrófagos, en tanto que la inmunoterapia puede estimular la acción antitumoral de los linfocitos”, dijo Wagner Wanderley.
Este descubrimiento es el resultado del doctorado del investigador de la UFC, quien realizó este estudio en colaboración con científicos del CRID en los laboratorios de este centro, hospedados en la Facultad de Medicina de Ribeirão Preto de la Universidad de São Paulo (FMRP-USP), en Brasil.
“Este estudio empezó con una idea sencilla. Ya se sabía que entre los efectos colaterales del paclitaxel se encontraba el dolor neuropático, relacionado con el receptor TLR4, y ahora creemos que este descubrimiento tiene un gran impacto en la clínica también”, dijo Thiago Mattar Cunha, profesor asociado de la FMRP-USP y uno de los autores del estudio.
Mattar Cunha explica que este trabajo comprendió la realización de experimentos en cultivo celular y en modelo animal, y análisis de bioinformática. En primer lugar, y para demostrar la actuación del medicamento en la respuesta inmunitaria innata, transformaron macrófagos in vitro en estadio inactivo (en reposo, denominados M0) en un modelo antiinflamatorio y protumoral denominado M2. Al aplicarles el paclitaxel, los macrófagos M2 fueron reprogramados con el perfil M1 (antitumoral).
Luego del estudio en cultivo celular, el grupo realizó los experimentos in vivo en ratones transgénicos deficientes con respecto al receptor TLR4 en los macrófagos.
“En esos casos, observamos que el quimioterapéutico perdió su efecto. Utilizamos un linaje tumoral resistente al paclitaxel y a su efecto antiproliferativo. Observamos que aun sin la acción antiproliferativa, el medicamento seguía modulando al sistema inmunológico”, dijo Mattar Cunha.
La mejor respuesta
Además de los experimentos in vitro e in vivo, los científicos también efectuaron análisis de bioinformática de muestras de tumores de pacientes con cáncer de ovarios a las que se les aplicó el tratamiento con el paclitaxel, existentes en un banco de datos de expresión génica.
“Al analizar las biopsias fue posible identificar genes característicos de macrófagos con perfil M1 (antitumoral) en los tumores tratados con el quimioterapéutico, lo que avala nuestra hipótesis”, dijo Mattar Cunha.
Los investigadores pretenden avanzar en los estudios y realizar ensayos clínicos con el quimioterapéutico.
“Trabajaremos en dos líneas: el estudio de otros medicamentos quimioterapéuticos más antiguos para ver si también poseen acción inmunitaria antitumoral y la realización de ensayos clínicos con el paclitaxel. En el CRID trabajamos con asesores internacionales que han mostrado interés en realizar investigaciones clínicas para saber si este medicamento funciona como adyuvante en las terapias”, dijo Fernando Queiroz Cunha, coordinador del CRID.
Queiroz Cunha explica que la asociación más interesante sería con las llamadas checkpoints therapies, inmunoterapias que bloquean las proteínas que impiden que el sistema inmunológico ataque a las células cancerígenas.
“Son tratamientos tendientes a mejorar la respuesta inmunitaria, y el efecto del paclitaxel es precisamente éste. Quizá pueda utilizárselo como terapia adyuvante contra otros tumores”, dijo.
Este descubrimiento puede tener también un efecto importante sobre el costo de los tratamientos. “Se estima que el costo total del tratamiento con inhibidores de checkpoint puede llegar en la actualidad a un millón de reales por paciente. En tanto, el costo de esas drogas más antiguas como el paclitaxel, que salió al mercado a comienzos de la década de 1990, es mucho más bajo. Con base en este descubrimiento, es posible proponer la combinación de fármacos en busca de algo más que lo previsto en el pasado”, dijo Roberto Lima-Junior, docente del departamento de Fisiología y Farmacología de la UFC, quien también participó en la investigación.
Puede leerse el artículo intitulado Paclitaxel reduces tumor growth by reprogramming tumor-associated macrophages to an M1- profile in a TLR4-dependent manner (doi: 10.1158/0008-5472.CAN-17-3480), de Carlos W. Wanderley, David F. Colon, João Paulo Mesquita Luiz, Francisco F. Oliveira, Paula R. Viacava, Caio A. Leche, Janaina A. Pereira, Camila M. Silva, Cassia R. Silva, Rangel L. Silva, Cesar A. Speck-Hernández, José M. Mota, José C. Alves-Filho, Roberto C. Lima-Júnior, Thiago M. Cunha y Fernando Q. Cunha, en el siguiente enlace: cancerres.aacrjournals.org/content/early/2018/08/11/0008-5472.CAN-17-3480.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





