


La terapia con células CAR-T les aporta esperanzas a las personas con tipos de cáncer de difícil tratamiento (ilustración: CTC-USP)
Inaugurado en 2022 con el apoyo de la FAPESP, el Nutera congrega a científicos del Instituto Butantan y del Hemocentro de Ribeirão Preto, vinculado a la Universidad de São Paulo. Se trata de la primera fábrica de productos celulares de Latinoamérica y es un potencial proveedor del SUS, la red nacional de salud pública
Inaugurado en 2022 con el apoyo de la FAPESP, el Nutera congrega a científicos del Instituto Butantan y del Hemocentro de Ribeirão Preto, vinculado a la Universidad de São Paulo. Se trata de la primera fábrica de productos celulares de Latinoamérica y es un potencial proveedor del SUS, la red nacional de salud pública
La terapia con células CAR-T les aporta esperanzas a las personas con tipos de cáncer de difícil tratamiento (ilustración: CTC-USP)
Por Maria Fernanda Ziegler | Agência FAPESP – Un ensayo clínico con las llamadas células CAR-T para el tratamiento del cáncer en la sangre aprobado por la Agencia Nacional de Vigilancia Sanitaria (Anvisa) de Brasil el pasado 27 de septiembre se pondrá en marcha en los próximos meses, con la participación de 81 voluntarios que aún no han sido seleccionados. Según los ideadores de este estudio, se trata del primer paso para transformar al Núcleo de Terapia Avanzada (Nutera) –la primera fábrica de productos celulares de América Latina, inaugurada en 2022 con el apoyo de la FAPESP– en un proveedor de productos destinados a terapias celulares avanzadas tales como las células CAR-T para el SUS −el Sistema Único de Salud−, las siglas con las cuales se la conoce en el país a la red nacional de salud pública.
La terapia con células CAR-T les aporta esperanza a las personas que padecen ciertos tipos de cáncer de difícil tratamiento. Es una técnica que científicos del Centro de Terapia Celular (CTC), un Centro de Investigación, Innovación y Difusión (CEPID) de la FAPESP con sede en la Universidad de São Paulo (USP) de la localidad de Ribeirão Preto, pusieron a prueba por primera vez en Latinoamérica, en el año 2019. En total, 17 pacientes han sido tratados en forma experimental en el CTC. Y en su mayoría han exhibido una remisión total de la enfermedad en un lapso de un poco más de un mes (lea más en: agencia.fapesp.br/31687).
Los ensayos clínicos comenzarían en los próximos meses con el objetivo de verificar la seguridad y la efectividad del tratamiento (en sus fases I y II) en personas con leucemia linfoide aguda de células B y linfoma no Hodgkin de células B. No obstante, como todavía falta la aprobación de la Comisión Nacional de Ética en la Investigación Científica (Conep, en portugués) para que se pongan en marcha, aún no se han determinado los perfiles de esos voluntarios.
Esta iniciativa se llevará adelante gratuitamente en cinco hospitales del estado de São Paulo, entre ellos el Hospital de Clínicas de la Facultad de Medicina de Ribeirão Preto (FMRP-USP) y el Hospital de Clínicas de la Facultad de Medicina de la USP en la ciudad de São Paulo (FM-USP).
“La aprobación de los ensayos es una etapa importante para la materialización de un plan mayor: la fabricación de productos celulares [células alteradas en laboratorio] destinadas al tratamiento de distintos tipos de cáncer y otras enfermedades. Es la primera vez que se distribuirán productos de esta complejidad íntegramente en Latinoamérica. Se trata de un avance enorme en el área de la biotecnología”, destaca Dimas Covas, director del Hemocentro de Ribeirão Preto y coordinador de la investigación.
Sucede que, aparte de aprobar los ensayos clínicos, Anvisa también autorizó la elaboración de productos celulares para la realización de los mismos. El Hemocentro de Ribeirão Preto, la USP y el Instituto Butantan suscribieron una colaboración que redundó en la construcción del Nutera, que contó con financiación a través del Programa de Centros de Ciencia para el Desarrollo (CCD) de la FAPESP (lea más en: agencia.fapesp.br/39064).
Solamente después de los resultados del estudio será posible solicitar ante Anvisa el permiso para la comercialización y la distribución de los productos celulares.
“La fábrica es una plataforma que permite manipular células genéticamente modificadas, tal como es el caso de las células CAR-T, vectores virales para la terapia génica y células derivadas de células madre pluripotentes. Se la construyó en un área pública, en un hospital que atiende casi en su totalidad a pacientes del SUS. Empezamos con el CAR-T19, que es el producto del momento, pero existe una pipeline con muchas investigaciones en marcha, con la segunda y la tercera generación de productos CAR-T, por ejemplo. Por ende, los ensayos clínicos constituyen solamente el comienzo de un proyecto que está siendo sumamente exitoso”, afirma Covas.
Actualmente, la fábrica posee una capacidad para atender 13 casos cada 34 días. “Aún no contempla toda la demanda del SUS. Pero esperamos que en un año sea posible atender 150 casos e ir incrementando ese número con el tiempo”, afirma Diego Clé, director médico del Hemocentro de Ribeirão Preto y uno de los investigadores participantes.
Célula por célula
Durante los ensayos clínicos, se extraerán los linfocitos (las células de defensa) de los voluntarios y se enviarán las muestras de sangre a la fábrica. Allí, mediante la aplicación de técnicas de bioingeniería, los científicos insertarán una secuencia genética de un vector viral en el ADN de esos linfocitos.
Con esa nueva secuencia de ADN, los linfocitos comienzan a expresar a una proteína nueva (de la cual carecían anteriormente), capaz de reconocer a los tumores.
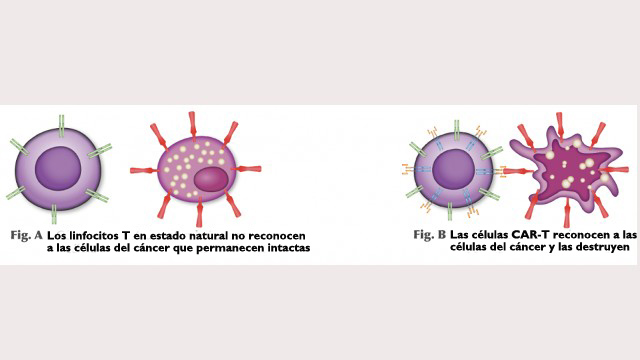
“El linfocito pasa a expresar a un receptor (el llamado CAR) en su superficie que reconoce la presencia de una proteína específica de la célula tumoral. En el caso de nuestro estudio, el receptor reconoce a la proteína CD19, que está presente en las células de la leucemia linfoide y del linfoma no Hodgkin”, explica Clé.
Una vez que están listos, se congelan los linfocitos y se los devuelve a los hospitales en donde se llevarán a cabo los ensayos clínicos. “A los pacientes se les aplican sus nuevos linfocitos como si fuera una transfusión de sangre. En ese momento, las células de defensa pasan a reconocer al tumor y a liberar una serie de mediadores inflamatorios para atacarlo”, dice el médico.
Más información en: www.hemocentro.fmrp.usp.br/terapia/.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





