


Científicos brasileños pusieron a prueba esta intervención en ratones. El estudio muestra que el estímulo dirigido de la producción de una proteína conocida como PKA promueve el crecimiento muscular y aumenta la resistencia a la fatiga (un ejemplo de electroporación; imagen: Dawit Gonçalves/FMRP-USP)
Científicos brasileños pusieron a prueba esta intervención en ratones. El estudio muestra que el estímulo dirigido de la producción de una proteína conocida como PKA promueve el crecimiento muscular y aumenta la resistencia a la fatiga
Científicos brasileños pusieron a prueba esta intervención en ratones. El estudio muestra que el estímulo dirigido de la producción de una proteína conocida como PKA promueve el crecimiento muscular y aumenta la resistencia a la fatiga
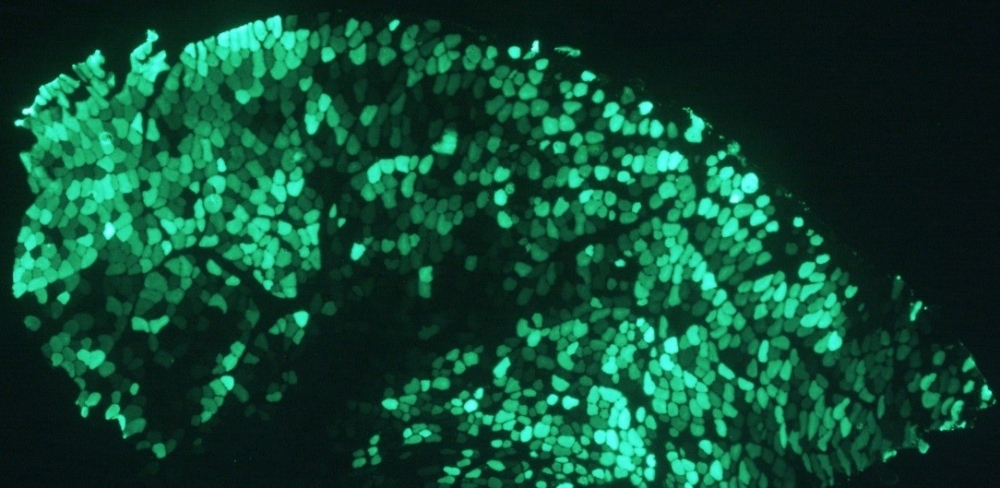
Científicos brasileños pusieron a prueba esta intervención en ratones. El estudio muestra que el estímulo dirigido de la producción de una proteína conocida como PKA promueve el crecimiento muscular y aumenta la resistencia a la fatiga (un ejemplo de electroporación; imagen: Dawit Gonçalves/FMRP-USP)
Por Maria Fernanda Ziegler | Agência FAPESP – Científicos de la Universidad de São Paulo (USP), en Brasil, demostraron por primera vez que el estímulo de la expresión de una proteína que el cuerpo humano produce naturalmente puede erigirse como una estrategia en el combate contra la pérdida de masa muscular esquelética, un proceso natural del envejecimiento que puede intensificarse en casos de enfermedades neurodegenerativas e inflamatorias, o entre personas que deben pasar largos períodos internadas en Unidades de Terapia Intensiva (UTI).
Se estima que 10 días de permanencia en UTI resultan en la pérdida de hasta un 20% de la masa muscular de las extremidades inferiores y también de músculos respiratorios importantes como el diafragma. En esos casos, existe una carencia de tratamiento medicamentoso. Aparte de la fisioterapia, los ejercicios respiratorios y las técnicas de electroestimulación, no existe ningún fármaco que no genere graves efectos colaterales que pueda revertir efectivamente este problema.
“Logramos demostrar que cuando se sobreexpresó la proteína quinasa A (PKA) en los músculos de los ratones, se produjo un aumento significativo de la resistencia a la fatiga muscular. Esto sucede porque aparte de suprimir la actividad de la FoxO, una proteína activadora de genes asociados a la atrofia, la PKA logra incrementar la formación de fibras musculares con mayor potencial oxidativo [mayor capacidad respiratoria], promoviendo así la hipertrofia y una mayor resistencia a la fatiga en músculos específicos”, dice Luiz Carlos Navegantes, docente del Departamento de Fisiología de la Facultad de Medicina de Ribeirão Preto (FMRP) de la USP y coautor de artículo publicado en la revista Faseb J.
Este hallazgo, fruto de estudio que contó con el apoyo de la FAPESP, le imprime una nueva orientación a la búsqueda de fármacos que protejan a los músculos contra la pérdida de masa muscular sin provocar efectos colaterales graves, tales como la hipertrofia del músculo cardíaco, taquicardia, infarto e incluso la muerte.
“El papel beneficioso de la PKA en los músculos, que consiste en estimular el anabolismo y la fuerza, es único entre todas las proteínas conocidas, lo que la convierte en un blanco estratégico y en objeto de estudios que apunten a combatir enfermedades neuromusculares y situaciones patológicas que llevan a la debilidad y a la atrofia muscular”, afirma.
Una relación metabólica
Hace 23 años, el grupo de investigadores de la FMRP-USP encabezado por la profesora Isis do Carmo Kettelhut descubrió que la hormona adrenalina, además de promover la rotura de fuentes energéticas tales como los lípidos y los hidratos de carbono, inhibía también la degradación de las proteínas que forman las fibras musculares. “Eso constituyó un cambio de paradigma, pues la adrenalina fue siempre tenida como una hormona movilizadora de energía y no como una capaz de evitar la rotura excesiva de proteínas, que sería catastrófica, sobre todo en lo concerniente a aquellas que mantienen la contracción de los músculos”, le explica Navegantes a Agência FAPESP.
Desde el descubrimiento de la acción protectora de la adrenalina sobre los músculos, el grupo de investigadores ha venido estudiando el potencial terapéutico de drogas similares a esta hormona (simpatomiméticos), aunque sin lograr evitar los efectos colaterales. “La preservación de las proteínas musculares es lo que el todo mundo anhela, desde el atleta que desea incrementar su masa muscular hasta el paciente que necesita que el diafragma funcione para seguir respirando normalmente. Pero esas drogas pueden tener efectos perjudiciales en el organismo e incluso ser fatales, a causa de la hipertrofia cardíaca”, dice.
Navegantes remarca que el principal problema relacionado con el uso de la adrenalina sintética o de simpatomiméticos reside en que esas sustancias poseen acción sistémica y sus efectos no pueden orientarse hacia la protección de un músculo solamente.
Esto fue lo que se probó en otro estudio de los científicos, cuando testearon el simpatomimético formoterol en el tratamiento crónico de la pérdida de masa y la fatiga muscular. En un artículo publicado en la revista Cachexia, Sarcopenia and Muscle, los investigadores describieron los efectos de esa droga, comúnmente utilizada en el tratamiento del asma, y demostraron que era también capaz de promover el crecimiento muscular y potenciar la fuerza de los músculos esqueléticos.
“El músculo crecía básicamente debido a dos mecanismos: por la acción directa de la droga al inhibir la degradación de las proteínas y a causa del aumento de la secreción de insulina, una hormona anabólica bastante conocida. Sin embargo, pese a ser sumamente interesantes en el combate contra la atrofia y a que ya se los ha adoptado en la clínica médica, los simpatomiméticos pueden causar efectos colaterales indeseables, fundamentalmente la hipertrofia cardíaca, lo que vuelve peligroso su uso crónico”, dice.
Con acción orientada
El estudio con la proteína PKA surgió como una posibilidad de solucionar este problema mediante la transferencia génica selectiva, es decir, la activación de un músculo específico únicamente.
“Ya se sabía que la PKA es activada por la adrenalina y, por ende, que está relacionada con la rotura de lípidos e hidratos de carbono, que constituyen nuestras fuentes de energía. Pero la PKA se ubica dentro de la célula muscular y la adrenalina es una hormona circulante. Y esta diferencia fue la que nos permitió orientar el efecto de la PKA hacia un determinado músculo de los ratones”, dice.
Navegantes hace hincapié en que, para que la adrenalina inhiba la degradación muscular –y también rompa lípidos e hidratos de carbono–, es necesario activar a la PKA. De este modo, la adrenalina se acopla a un receptor de la membrana celular y envía una señal que promueve la estimulación de la PKA en el citosol (el líquido que ocupa el citoplasma). Entre los diversos efectos finales mediados por la PKA, se produce dentro del núcleo de la célula la supresión de los genes ligados a la atrofia.
Para evaluar los efectos de la proteína en un solo músculo de los ratones, los investigadores utilizaron una técnica de interferencia génica selectiva (electroporación), a los efectos de activar genes asociados con la producción de la proteína PKA de manera orientada y no en todas las células del organismo.
Con esta técnica, mediante la aplicación de un impulso eléctrico, se introduce en el músculo del animal vivo un plásmido, que se incorpora y así se modifica el ADN de la fibra muscular. Este método fue aprendido por el doctorando Dawit Albieiro Pinheiro Gonçalves durante una pasantía de investigación realizada en Italia con el apoyo de la FAPESP.
“Es una técnica utilizada para comprobar hipótesis en animales vivos. Consiste en aplicar un pulso eléctrico en el músculo estudiado e introducir así un plásmido que funciona como un vector capaz de modificar los genes [mediante edición genética] en las células de ese músculo específico, produciendo de ese modo determinadas proteínas de interés; en este caso, la PKA. Así es posible interferir selectivamente en un músculo esquelético específico sin alterar los otros tejidos de los animales”, explica Navegantes.
El investigador explica que esta intervención resultó en la sobreexpresión de la PKAcat –una subunidad catalítica del PKA– y en el consiguiente aumento de la conversión de fibras con potencial oxidativo, mejorando considerablemente la resistencia del músculo a la fatiga muscular. “Cuando hicimos lo contrario, es decir, la electroporación con una molécula denominada PKI, que inhibe a la PKA endógena, observamos que hubo una activación de genes relacionados con la atrofia y la reducción del área de las fibras musculares”, afirma.
El descubrimiento de la acción de la proteína en la protección de las fibras musculares hace posible la investigación de nuevos fármacos. “A través de la electroporación, logramos probar que la PKA endógena inhibe la pérdida de masa muscular. Nuestro objetivo ahora consiste en estudiar fármacos que activen a la PKA y también en realizar estudios de envejecimiento y de enfermedades neurodegenerativas mediante colaboraciones, en modelos clínicos y experimentales”, dice.
Puede leerse el artículo cAMP-dependent protein kinase inhibits FoxO activity and regulates skeletal muscle plasticity in mice (doi: 10.1096/fj.201902102RR), de Wilian A. Silveira, Dawit A. Gonçalves, Juliano Machado, Natalia Lautherbach, Danilo Lustrino, Silvia Paula-Gomes, Marcelo G. Pereira, Elen H. Miyabara, Marco Sandri, Isis C. Kettelhut y Luiz C. Navegantes, en el siguiente enlace: https://faseb.onlinelibrary.wiley.com/doi/full/10.1096/fj.201902102RR.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





