

Científicos de un centro de investigación apoyado por la FAPESP revelan que una proteína llamada gasdermina D participa en el proceso de lesión de los órganos en pacientes sépticos. Este trabajo muestra también que un medicamento originariamente recomendado para el tratamiento de alcohólicos puede inhibir la acción de esta molécula y prevenir complicaciones (una imagen de microscopía muestra las NET en blanco y la proteína gasdermina D en rojo; crédito: CRID/USP).
Científicos de un centro de investigación apoyado por la FAPESP revelan que una proteína llamada gasdermina D participa en el proceso de lesión de los órganos en pacientes sépticos. Este trabajo muestra también que un medicamento originariamente recomendado para el tratamiento de alcohólicos puede inhibir la acción de esta molécula y prevenir complicaciones.
Científicos de un centro de investigación apoyado por la FAPESP revelan que una proteína llamada gasdermina D participa en el proceso de lesión de los órganos en pacientes sépticos. Este trabajo muestra también que un medicamento originariamente recomendado para el tratamiento de alcohólicos puede inhibir la acción de esta molécula y prevenir complicaciones.
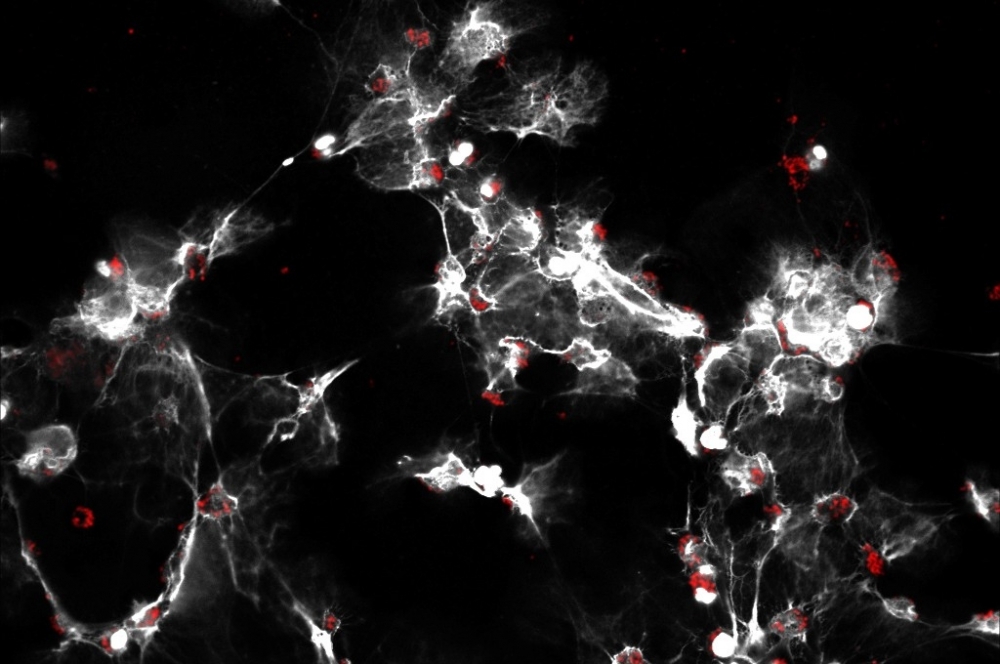
Científicos de un centro de investigación apoyado por la FAPESP revelan que una proteína llamada gasdermina D participa en el proceso de lesión de los órganos en pacientes sépticos. Este trabajo muestra también que un medicamento originariamente recomendado para el tratamiento de alcohólicos puede inhibir la acción de esta molécula y prevenir complicaciones (una imagen de microscopía muestra las NET en blanco y la proteína gasdermina D en rojo; crédito: CRID/USP).
Karina Toledo | Agência FAPESP – Investigadores de la Universidad de São Paulo (USP) y colaboradores dieron a conocer una nueva estrategia destinada a prevenir complicaciones asociadas a la sepsis en un artículo publicado en la revista Blood.
La propuesta consiste en inhibir la acción de una proteína llamada gasdermina D, cosa que los autores demostraron que es posible con un medicamento aprobado para uso humano y originariamente recomendado para combatir la dependencia de alcohol: el disulfiram.
Este trabajo se llevó a cabo en el Centro de Investigaciones en Enfermedades Inflamatorias (CRID), un Centro de Investigación, Innovación y Difusión (CEPID) de la FAPESP con sede en la Facultad de Medicina de Ribeirão Preto (FMRP-USP).
“Sabemos que este fármaco es seguro, pues se encuentra en uso desde la década 1950, y estamos proponiendo su reposicionamiento para el tratamiento de la sepsis. Vimos que funciona en las pruebas in vitro y en animales. Ahora es necesario realizar un ensayo clínico para evaluar su eficacia en pacientes sépticos”, le dice a Agência FAPESP Camila Meirelles Silva, posdoctoranda en el CRID y primera autora del artículo.
La sepsis, popularmente conocida como “infección generalizada”, es en realidad una inflamación sistémica comúnmente desencadenada por una infección bacteriana que sale de control. En el intento de combatir a los patógenos, el sistema inmunitario termina perjudicando al propio organismo. En las formas más graves, los pacientes desarrollan lesiones que comprometen el funcionamiento de órganos vitales, fundamentalmente los pulmones.
En trabajos anteriores, el equipo del CRID había revelado que un mecanismo inmunitario conocido como “trampa o malla extracelular de neutrófilos” (NET, por sus siglas en inglés) está directamente implicado en las lesiones tisulares de los pacientes con sepsis. Tal como el propio nombre lo sugiere, NET es una estrategia de defensa que emplean principalmente los neutrófilos, un tipo de leucocitos capaces de fagocitar bacterias, hongos y virus. En algunas situaciones extremas, estas células inmunitarias se mueren y el material existente en su núcleo es arrojado al medio exterior en la forma de mallas que son tóxicas tanto para los patógenos como para las células del organismo.
“En este nuevo trabajo hemos develado el mecanismo que permite la liberación de las NET, en el cual la gasdermina D está directamente implicada. Asimismo, demostramos que, al impedir que los neutrófilos liberen estas mallas mediante la inhibición de la gasdermina D, logramos reducir el nivel de lesión tisular y mejorar el pronóstico”, comenta Meirelles Silva.
La metodología
Una parte de los experimentos se llevó a cabo con leucocitos aislados en pacientes con sepsis internados hacía 24 horas: eran 12 varones y 12 mujeres. Los análisis realizados en el microscopio confocal mostraron las NET siendo liberadas in vitro por gran parte de esas células. Las pruebas también indicaron que en los neutrófilos de los pacientes había una gran cantidad de gasdermina D en su forma activa, tal como se lo observó en los neutrófilos aislados en ratones sépticos.
“La gasdermina D es una proteína formadora de poros. Trabajos anteriores demostraron que, cuando esa molécula se activa en las células, forma poros [orificios] en la membrana nuclear que permiten la salida del material genético hacia el citosol. Luego la gadermina D abre otros poros en la membrana plasmática, lo que hace posible la liberación de todo ese contenido hacia el medio extracelular. Nosotros comprobamos que en la sepsis la proteína también actúa de este modo”, informa Meirelles Silva.
Los experimentos in vivo se llevaron a cabo con ratones sometidos a un procedimiento destinado a inducir un cuadro de sepsis. Parte de los animales expresaba normalmente la gasdermina D. Y otro grupo estaba compuesto por roedores genéticamente modificados para no producir esa proteína en ninguna célula del cuerpo (ratones KO para gasdermina D).
“Cuando inducimos la sepsis, observamos que los animales KO producían una menor cantidad de NET, desarrollaban menos lesiones de órganos [no padecían edema pulmonar, a diferencia de los restantes] y sobrevivían más”, comenta la investigadora.
Las pruebas in vitro con las células de los ratones KO confirmaron que aun en presencia de LPS –una molécula presente en la membrana de bacterias patogénicas que el sistema inmunitario suele interpretar como señal de peligro–, los neutrófilos no se rompen y no sueltan sus trampas.
Pruebas de inhibición
Los datos existentes en la literatura científica indicaban que el disulfiran posee la capacidad de unirse a la gasdermina D e impedir que la proteína forme poros en las membranas de las células. Con base en esas evidencias, los científicos del CRID decidieron poner a prueba el efecto de este fármaco en el contexto de la sepsis, una enfermedad para la cual aún no existe un medicamento específico.
En las pruebas in vitro, los investigadores observaron que, tras el tratamiento con el fármaco, tanto los neutrófilos humanos cuanto los de ratones dejaban de liberar NET cuando se los estimulaba con LPS.
En otro experimento, los neutrófilos aislados en pacientes sépticos se incubaron con el medicamento y fue posible observar que el tratamiento inhibió el proceso de liberación de las mallas de neutrófilos.
Por último, se trató a los ratones con sepsis con disulfiran y se comparó su evolución con la de roedores no tratados.
En los animales a los que se les aplicó el fármaco, se observaron menos lesiones tisulares (incluso menos edema pulmonar), menor cantidad de NET en la sangre y un mejor pronóstico (un 60 % sobrevivió, ante un 20 % en el grupo no tratado).
Los resultados suscitaron el interés de la comunidad científica y motivaron un comentario también publicado en Blood de los investigadores de Alemania Maksim Klimiankó y Julia Skokowa, ambos del University Hospital Tuebingen.
“Los neutrófilos aplican múltiples formas de defensa contra los patógenos, lo que incluye a la fagocitosis, la producción de especies reactivas de oxígeno, la secreción de enzimas bactericidas y formación de NET. Y pagan un alto precio por todas esas acciones defensivas: mueren durante el proceso de digerir, neutralizar y matar a los invasores. Sin embargo, no todo es perfecto en esa línea de defensa, ya que es casi imposible regular el grado de activación de los neutrófilos. Una vez que se activan, suelen exhibir fenotipos hipersensibles, lo que causa efectos deletéreos tanto en el lugar de la inflamación como sistémicamente, y cumplen un papel esencial en el comienzo del proceso de disfunción de múltiples órganos y en la letalidad de la sepsis. El ataque a los mecanismos responsables de los efectos deletéreos de los neutrófilos durante la sepsis, preservando otras funciones de estas células, puede constituir una terapia valiosa”, afirman los alemanes en la revista.
Los resultados de esta investigación también constituyeron el tema de un pódcast producido por el equipo de Blood.
Los próximos pasos
Fernando de Queiroz Cunha, docente de la FMRP-USP y coordinador del CRID, comenta que el hecho de que la producción haya cesado en Brasil en 2019 le dificultó al grupo la realización de un ensayo clínico.
“Era un medicamento tan barato que la empresa resolvió sacarlo del mercado, y en la actualidad los psiquiatras que tratan a los alcohólicos deben importarlo. Como alternativa, estamos negociando con una farmacéutica nacional el desarrollo de una molécula ligeramente modificada, que podría patentarse y ponerse a disposición en el mercado nacional”, comenta.
De Queiroz Cunha revela a su vez que el equipo del CRID pretende verificar si el disulfiran puede aplicarse para prevenir lesiones en órganos de pacientes con COVID-19. Un estudio anterior del grupo mostró que las NET participan en el cuadro de inflamación descontrolada que desencadena el SARS-CoV-2 (lea más en: https://agencia.fapesp.br/33534/).
Puede leerse el artículo Gasdermin D inhibition prevents multiple organ dysfunction during sepsis by blocking NET formation en el siguiente enlace: https://ashpublications.org/blood/article-abstract/138/25/2702/476604/Gasdermin-D-inhibition-prevents-multiple-organ?redirectedFrom=fulltext.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





