

Matriz extracelular de un hígado descelularizado. Luego del proceso de descelularización controlada, los investigadores obtienen dicha matriz que se emplea para la reconstrucción hepática (foto: CEGH-CEL/USP)
Es un método elaborado en el Centro de Estudios del Genoma Humano y de Células Madre de Brasil, y puede permitir escalar la fabricación de órganos para la realización de trasplantes
Es un método elaborado en el Centro de Estudios del Genoma Humano y de Células Madre de Brasil, y puede permitir escalar la fabricación de órganos para la realización de trasplantes
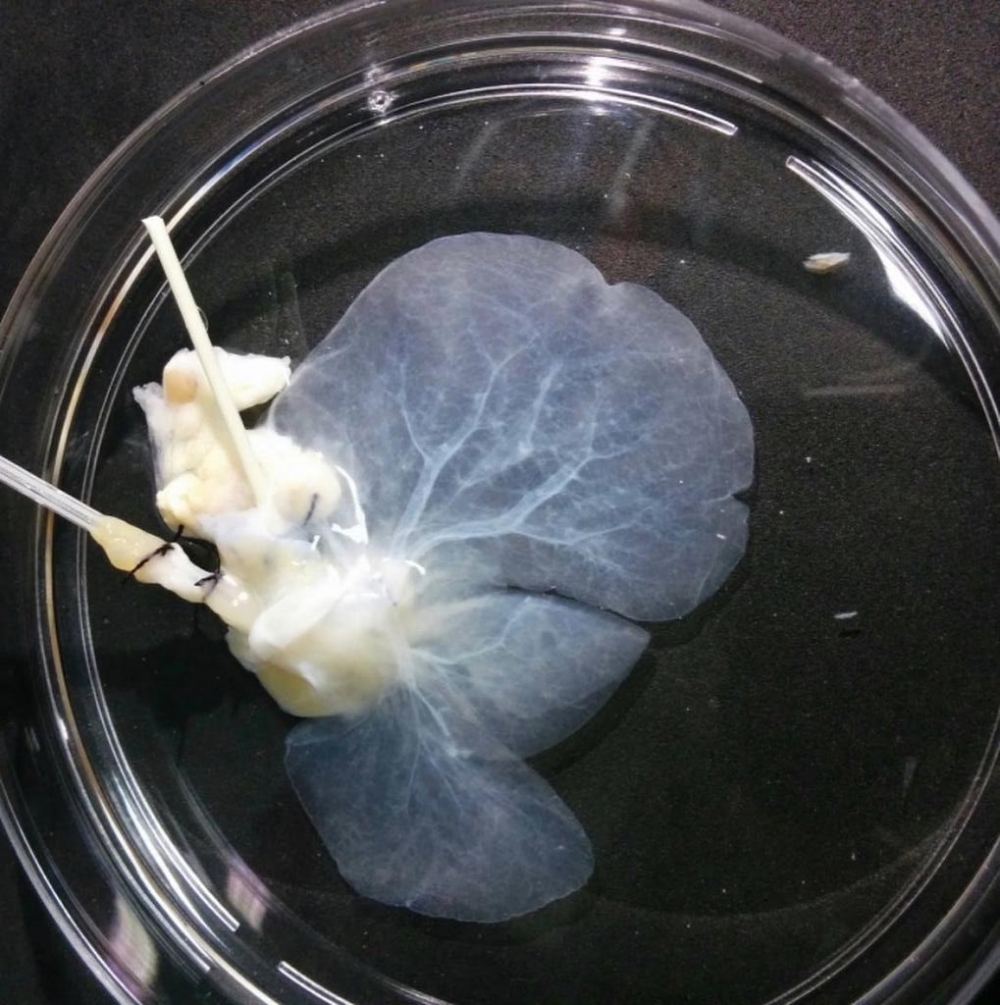
Matriz extracelular de un hígado descelularizado. Luego del proceso de descelularización controlada, los investigadores obtienen dicha matriz que se emplea para la reconstrucción hepática (foto: CEGH-CEL/USP)
Por Elton Alisson | Agência FAPESP – Científicos del Centro de Estudios del Genoma Humano y de Células Madre (CEGH-CEL), del Instituto de Biociencias de la Universidad de São Paulo (IB-USP), en Brasil, desarrollaron una técnica para la reconstrucción y la producción de hígados en laboratorio.
La prueba de concepto de este método se concretó con hígados de ratas. Durante la próxima etapa del estudio, los investigadores pretenden adaptar la técnica con el objetivo de producir en el futuro hígados humanos, con miras a incrementar la disponibilidad de estos órganos para la realización de trasplantes.
Los resultados de este estudio, que cuenta con el apoyo de la FAPESP, salieron publicados en la revista Materials Science and Engineering: C.
“La idea es producir hígados humanos en laboratorio y a escala con el objetivo de disminuir la espera de donantes compatibles y los riesgos de rechazo de los órganos trasplantados”, le dice a Agência FAPESP Luiz Carlos de Caires Júnior, primer autor del estudio. El investigador lleva adelante su posdoctorado en el CEGH-CEL, un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la FAPESP.
Esta metodología se basa en técnicas de bioingeniería de tejidos desarrolladas durante los últimos años que apuntan a la producción de órganos destinados a trasplantes, y denominadas descelularización y recelularización.
Estas técnicas consisten en someter a los órganos de donantes fallecidos –en este caso, el hígado– a sucesivos lavados con soluciones detergentes o enzimas, con el objetivo de extraer todas las células de los tejidos hasta que quede únicamente la matriz extracelular con la estructura y la forma original de dichos órganos. La matriz extracelular se recompone entonces con células derivadas del paciente receptor, a los efectos de evitar el riesgo de que aparezcan reacciones inmunológicas y para disminuir el riesgo de rechazo del órgano trasplantado a largo plazo.
“Es como si se trasplantase en el receptor un hígado recauchutado al que este no lo rechazaría, pues se lo reconstituyó con sus propias células. Ni siquiera necesitaría tomar medicamentos inmunosupresores”, explica Mayana Zatz, coordinadora del CEGH-CEL y coautora del estudio.
Por medio de estas técnicas también es posible reconstituir órganos considerados limítrofes, aumentando a su disponibilidad para los pacientes en la fila de espera, explica De Caires.
“Muchos órganos disponibles para trasplantes no se aprovechan porque provienen de personas que sufrieron accidentes de tránsito. Con estas técnicas es posible recuperarlos, dependiendo de las condiciones en que se encuentren”, afirma el investigador.
Con todo, el proceso de descelularización remueve los principales componentes de la matriz extracelular de los órganos, tales como moléculas que les indican a las células que deben proliferar y formar vasos. De este modo, compromete la recelularización del tejido y disminuye las propiedades de adherencia de las células a la matriz extracelular.
Para superar este obstáculo, los investigadores del CEGH-CEL perfeccionaron las técnicas de descelularización y recelularización al introducir una nueva etapa.
Después de aislar y descelularizar hígados de ratas, los investigadores les inyectaron en la matriz extracelular una solución rica en moléculas tales como las proteínas Sparc y TGFB1, producidas por células hepáticas cultivadas en laboratorio en un medio condicionado. Estas proteínas les indican a las células hepáticas que deben proliferar y formar vasos sanguíneos, funciones esenciales para el buen funcionamiento del hígado.
“El enriquecimiento de la matriz extracelular con estas moléculas permite que la misma quede mucho más parecida a la de un hígado sano”, afirma De Caires.
Tras tratar a la matriz extracelular de hígados de ratas con esta solución, se introdujeron en el material hepatocitos y células endoteliales y mesenquimales, estas últimas producidas con base en células madre pluripotentes inducidas (iPS, por sus siglas en inglés). Este método consiste en reprogramar células adultas (provenientes de la piel o de otro tejido de fácil acceso) para hacerlas asumir el estadio de pluripotencia similar al de células madre embrionarias.
“Este trabajo demostró que es posible inducir la diferenciación de células madre humanas en linajes de células que forman parte de un hígado y utilizarlas para reconstruir el órgano, de manera tal de volverlo funcional. Es la primera prueba de concepto de que esta técnica funciona”, sostiene Zatz.
Con la ayuda de una bomba de jeringa, se introdujeron las células hepáticas en la matriz extracelular de hígados de ratas para producir órganos con las características del órgano humano.
Los órganos crecieron durante cinco semanas en una incubadora que simula las condiciones de un cuerpo humano. Los análisis indicaron que el enriquecimiento de la matriz extracelular con la solución rica en proteínas Sparc y TGFB1 mejoró mucho la recelularización de los hígados producidos.
“Las células hepáticas crecen y funcionan mejor con este tratamiento. Ahora pretendemos construir un biorreactor para concretar la descelularización de hígados humanos y evaluar la posibilidad de producirlos en laboratorio y escalarlos”, dice De Caires.
Según el investigador, esta técnica también puede adaptarse para la producción en laboratorio de otros órganos, tales como pulmones, corazones y piel.
La fabricación de órganos
Este proyecto integra una de las líneas de investigación del CEGH-CEL orientada hacia la fabricación o la reconstrucción de órganos para trasplantes mediante el empleo de diferentes técnicas.
En el marco de un proyecto desarrollado en colaboración con la compañía farmacéutica EMS y que cuenta con el apoyo por la FAPESP a través del Programa de Apoyo a la Investigación en Asociación para la Innovación Tecnológica (PITE), los investigadores del Centro pretenden modificar órganos de cerdos, tales riñones, corazones y piel, para trasplantárselos a humanos (lea más en: agencia.fapesp.br/29784/).
Como no es posible trasplantar hígados de cerdos a humanos, los científicos diseñaron otras estrategias: la descelularización y la recelularización y la producción de órganos mediante impresión 3D (lea más en: agencia.fapesp.br/32287/).
“Estos distintos frentes de estudio son complementarios. En el futuro, esperamos poder contar con fábricas de órganos para trasplantes”, dice Zatz.
Puede leerse el artículo intitulado Pre-coating decellularized liver with HepG2-conditioned medium improves hepatic recellularization (DOI: 10.1016/j.msec.2020.111862), de Luiz Carlos de Caires-Júnior, Ernesto Goulart, Kayque Alves Telles-Silva, Bruno Henrique Silva Araujo, Camila Manso Musso, Gerson Kobayashi, Danyllo Oliveira, Amanda Assoni, Valdemir Melechco Carvalho, Antônio Fernando Ribeiro-Jr, Renata Ishiba, Karina Andrighetti Oliveira Braga, Natalia Nepomuceno, Elia Caldini, Thadeu Rangel, Silvano Raia, Peter I. Lelkes y Mayana Zatz, en la revista Materials Science and Engineering: C, en el siguiente enlace: www.sciencedirect.com/science/article/abs/pii/S0928493120337814.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





