


Blastocisto de camundongo (estrutura muito semelhante ao de humano). Em magenta, uma ampla expressão da proteína STIP1. Os núcleos das células estão corados em azul. O blastocisto representa um momento único no desenvolvimento, quando o embrião forma sua primeira estrutura organizada (imagem: Lopes et al./ICB-USP)
Liderados por cientistas da USP, os estudos ajudam a compreender o papel da STIP1 e da maspina em processos vitais das células e abrem caminho para avanços ligados ao câncer e a aplicações em medicina regenerativa
Liderados por cientistas da USP, os estudos ajudam a compreender o papel da STIP1 e da maspina em processos vitais das células e abrem caminho para avanços ligados ao câncer e a aplicações em medicina regenerativa
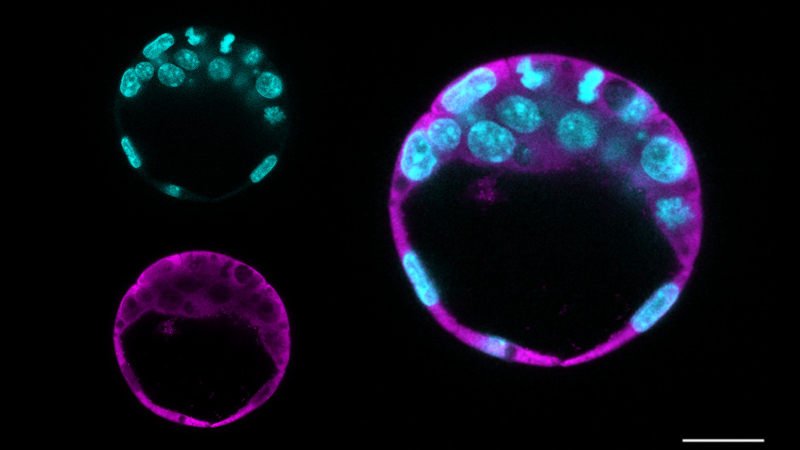
Blastocisto de camundongo (estrutura muito semelhante ao de humano). Em magenta, uma ampla expressão da proteína STIP1. Os núcleos das células estão corados em azul. O blastocisto representa um momento único no desenvolvimento, quando o embrião forma sua primeira estrutura organizada (imagem: Lopes et al./ICB-USP)
Luciana Constantino | Agência FAPESP – Duas pesquisas lideradas por cientistas brasileiras revelam papéis-chave de proteínas multifuncionais – a STIP1 e a maspina – em processos vitais para o funcionamento das células.
Os resultados demonstram novas funções proteicas que ajudam a compreender como as células mantêm sua forma, se comunicam e se renovam. Contribuem, assim, para novos estudos sobre câncer, embriogênese e potenciais aplicações em medicina regenerativa.
De acordo com um dos trabalhos, a STIP1 se apresenta como uma peça central no desenvolvimento embrionário e na manutenção da pluripotência (capacidade da célula se multiplicar e dar origem a outros tipos celulares).
Presente no organismo desde os primeiros estágios de vida, a STIP1 (sigla em inglês para stress inducible protein 1) é considerada essencial na manutenção do equilíbrio proteico dentro das células (homeostase). Atua como uma espécie de ponte, ajudando outras proteínas, chamadas chaperonas moleculares, a interagir e transferir suas “cargas” (proteínas-cliente) para que sejam processadas.
A outra pesquisa mostrou que a maspina atua na morfologia das células, como reguladora do citoesqueleto, e na adesão epitelial. A proteína é descrita na literatura científica como um supressor tumoral por sua função na prevenção do avanço e da disseminação da doença no organismo. Por isso, é um importante alvo relacionado ao câncer, especialmente ao de mama.
Ambos os artigos foram publicados na mesma edição da revista Communications Biology, do grupo Nature, sob a coordenação de cientistas do Departamento de Biologia Celular e do Desenvolvimento do Instituto de Ciências Biomédicas da Universidade de São Paulo (ICB-USP).
“Nosso trabalho é voltado à pesquisa básica, um caminho que demanda tempo, dedicação e continuidade até que os resultados se consolidem. Muitos alunos e pesquisadores participam dessa trajetória, e cada um deixa sua marca no avanço do conhecimento. Ver esse esforço coletivo se transformar em uma publicação é extremamente gratificante. É a certeza de que estamos contribuindo para a construção da ciência”, diz à Agência FAPESP Marilene Hohmuth Lopes, professora do ICB-USP e coordenadora do estudo sobre STIP1.
Já Nathalie Cella, também docente do ICB-USP e autora correspondente do artigo sobre maspina, destaca a importância de investir em pesquisa no longo prazo. “Avanços como esses só se concretizam com investimento contínuo em ciência básica e na formação de jovens pesquisadores”, avalia.
‘Guardiã da pluripotência’
Usando camundongos geneticamente modificados, o grupo de cientistas liderado por Lopes descobriu que a STIP1 é essencial para manter as células-tronco em seu estado primitivo, ou seja, aquele em que podem se transformar em qualquer tipo de tecido.
Ao analisar células-tronco embrionárias de murinos, os cientistas detectaram que a diminuição da proteína levou à perda de pluripotência. As células também ficaram mais vulneráveis ao estresse e apresentaram instabilidade genética.
Quando a proteína foi aumentada, o efeito foi o oposto: mais crescimento, resistência e manutenção da identidade das células-tronco.
Resultado da tese de doutorado de Camila Felix de Lima Fernandes, que recebeu bolsa da FAPESP, o estudo demonstrou que STIP1 é indispensável para o desenvolvimento embrionário, controlando a estabilidade genômica, a sobrevivência celular e a expressão de genes de pluripotência, abrindo caminho para a busca de estratégias em medicina regenerativa.
Surgida a partir do final dos anos 1990, essa vertente da medicina procura formas de recuperar e regenerar tecidos, órgãos e outras estruturas danificadas do organismo humano, seja por trauma ou doença. “Descobrimos que STIP1 atua como uma espécie de guardiã das células-tronco, garantindo que o maquinário celular funcione com precisão durante as fases mais delicadas da vida”, afirma Lopes.
Versatilidade
No caso da maspina, os pesquisadores descobriram que a proteína atua diretamente na sustentação da célula. Ela se liga às estruturas internas, responsáveis por dar forma e estabilidade.
O grupo combinou abordagens proteômicas, análises funcionais e de imagem. Detectou que, ao reduzir a presença da maspina nas células que revestem superfícies do corpo (epiteliais), elas perdem parte do contato entre si e mudam de forma.
A pesquisa também mostrou que a proteína controla o crescimento de filamentos que organizam o interior das células, funcionando como uma espécie de organizador estrutural que assegura a integridade dos tecidos.
Fruto do doutorado de Luiz Eduardo da Silva, iniciado pouco antes da pandemia de COVID-19, em 2020, o estudo ajuda a explicar os motivos de a maspina poder desempenhar papel oposto dependendo do contexto celular, funcionando como protetor ou como promotor de câncer.
“Nossa trajetória com a maspina mostra como a ciência básica, quando guiada pela curiosidade e persistência, pode revelar novos aspectos de proteínas já conhecidas e redefinir conceitos estabelecidos”, completa Cella, ao contar que “herdou” há mais de 20 anos o interesse pela proteína quando fez pós-doutorado no laboratório do professor Ming Zhang, na Baylor College of Medicine, nos Estados Unidos.
A FAPESP também apoiou os estudos por meio de outros 20 projetos (21/12268-4, 18/15553-9, 23/08391-0, 21/13114-0, 19/06971-4, 21/13070-3, 20/05443-1, 22/14445-3, 14/17385-5, 19/14952-0, 21/05287-2, 22/08106-1, 20/10671-3, 19/12710-9, 19/11097-1, 17/26158-0, 18/14933-2, 11/13906-2, 18/15557-4 e 19/00341-9).
Os artigos Stress-inducible phosphoprotein 1 (STIP1) is a critical stemness regulator in mouse embryonic stem cells and early mammalian development e Maspin/SerpinB5 is a cytoskeleton-binding protein that regulates epithelial cell shape podem ser lidos, respectivamente, em: nature.com/articles/s42003-025-08763-9 e nature.com/articles/s42003-025-08688-3.
Republicar
A Agência FAPESP licencia notícias via Creative Commons (CC-BY-NC-ND) para que possam ser republicadas gratuitamente e de forma simples por outros veículos digitais ou impressos. A Agência FAPESP deve ser creditada como a fonte do conteúdo que está sendo republicado e o nome do repórter (quando houver) deve ser atribuído. O uso do botão HMTL abaixo permite o atendimento a essas normas, detalhadas na Política de Republicação Digital FAPESP.





