

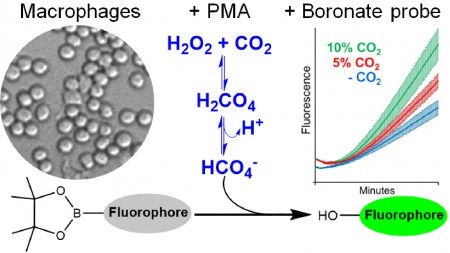
El trabajo se concretó en el Centro de Investigaciones en Procesos Redox en Biomedicina y resultó en la detección del peroximonocarbonato por primera vez en las células humanas (figura: Chem. Res. Toxicol 2024)
Se trata de un estudio realizado en la Universidad de São Paulo, en Brasil, que puede ayudar a entender el impacto de los niveles elevados de dióxido de carbono atmosféricos sobre la salud humana
Se trata de un estudio realizado en la Universidad de São Paulo, en Brasil, que puede ayudar a entender el impacto de los niveles elevados de dióxido de carbono atmosféricos sobre la salud humana

El trabajo se concretó en el Centro de Investigaciones en Procesos Redox en Biomedicina y resultó en la detección del peroximonocarbonato por primera vez en las células humanas (figura: Chem. Res. Toxicol 2024)
Agência FAPESP* – Los niveles elevados de dióxido de carbono (CO2) en la atmósfera no solamente pueden alterar el clima del planeta, sino también hacer lo propio en lo que concierne al funcionamiento de las células humanas. Sucede que este gas entra en interacción con el peróxido de hidrógeno (H₂O₂), que cumple diversas funciones en el organismo, dando origen a un compuesto oxidante conocido como peroximonocarbonato.
“Se están acumulando evidencias que indican que el peroximonocarbonato es importante tanto en las respuestas adaptativas de las células, que constituyen una señalización redox, como en las disfunciones celulares. También hay evidencias epidemiológicas de que los niveles de CO2 que se están por alcanzar en las sociedades contemporáneas urbanas provocan una serie de problemas fisiológicos. Y todavía se conoce poco acerca de los mecanismos de toxicidad del CO2”, comenta Ohara Augusto, docente del Instituto de Química de la Universidad de São Paulo (IQ-USP), en Brasil.
La investigadora coordinó un estudio publicado en la revista Chemical Research in Toxicology, en el cual se describe un nuevo método para detectar la presencia de peroximonocarbonato en las células basado en el empleo de sondas moleculares fluorescentes. Se trata de la primera vez que se detecta esta sustancia en las células. La referida investigación se concretó en el ámbito del Centro de Investigaciones en Procesos Redox en Biomedicina (Redoxoma), un Centro de Investigación, Innovación y Difusión (CEPID) financiado por la FAPESP.
“Este trabajo es importante no solamente porque suministra un método para demostrar que el peroximonocarbonato está produciéndose en una serie de condiciones, incluso celulares, sino también para discutirlo teniendo en cuenta la escasa atención que se le ha dado al CO2 en el área de redox", afirma Augusto.
Mediciones de fluorescencia
Para detectar el peroximonocarbonato, los investigadores efectuaron mediciones de fluorescencia con sondas de boronato. Primeramente, generaron concentraciones fisiológicas de peróxido de hidrógeno en estado estacionario en una reacción enzimática en producción constante, y midieron la fluorescencia de una sonda de boronato en presencia y en ausencia de CO2. Los boronatos se emplean para detectar oxidantes tales como peróxido de hidrógeno, peroxinitrito, ácido hipocloroso y peroximonocarbonato, que reaccionan con ellos a distintas velocidades y en diferentes intensidades permitiendo así la detección de esos oxidantes.
El estudio en las células fue concretó con macrófagos activados para generar peróxido de hidrógeno. Los macrófagos son células del sistema inmunitario que genera distintos oxidantes dependiendo del tipo de activación.
Los investigadores concretaron varios controles para arribar a la conclusión de que las células no estaban generando ni peroxinitrito ni ácido hipocloroso sino peroximonocarbonato en presencia de CO2.
“Éste es un método relativamente sencillo para detectar el peroximonocarbonato en concentraciones fisiológicas de peróxido de hidrógeno y CO2. Antes esto era imposible, pero en la actualidad los científicos pueden considerar que algunos efectos que observan en las células, como una mayor oxidación de determinadas proteínas o respuestas celulares, pueden deberse al peroximonocarbonato; y podrán ponerlo a prueba”, comenta la profesora del IQ-USP.
Si bien se trata de un oxidante que los químicos conocen desde la década de 1960 y que tiene aplicaciones tecnológicas como desinfectante y blanqueador, no se consideraba que el peroximonocarbonato pudiese formarse en las células debido a las bajas concentraciones de sus precursores y a su velocidad de formación. Augusto comenta que solamente a partir de la década de 2000 se empezó a investigar a este oxidante en los sistemas biológicos, aunque inicialmente el enfoque recaía sobre el daño oxidativo.
La señalización redox y el CO2
La señalización redox es una respuesta adaptativa. “Cuando se produce un ligero aumento del estrés, las células se adaptan. La formación de oxidantes puede hacer que genes de enzimas antioxidantes se expresen para responder en este caso al estrés oxidativo, por ejemplo. Y muchas vías que derivan en respuestas celulares comprenden tiol proteínas que el peroximonocarbonato oxida más rápido que el peróxido de hidrógeno", explica Augusto, quien a su vez añade que daño el celular irreversible solamente se plasma cuando la formación de oxidantes es muy grande.
El dióxido de carbono es uno de los precursores del peroximonocarbonato junto con el peróxido de hidrógeno. Este gas se encuentra naturalmente presente en la atmósfera y es un constituyente normal del cuerpo humano, que exhala alrededor de un kilo de CO2 diariamente como producto del metabolismo.
Desde el punto de vista redox, el CO2 modula la reactividad tanto del peróxido de hidrógeno cuanto del peroxinitrito, dos importantes metabolitos del oxígeno molecular. Además, altera la expresión de genes, incluidos los implicados en la inflamación, y participa en la nitración de proteínas vía peroxinitrito, y en la cabamilación de proteínas, otra modificación postraducción que puede alterar la función biológica de las proteínas.
Si bien se hacen necesarias otras evidencias de su papel como oxidante biológico, el peroximonocarbonato aparece como uno de los posibles intermediarios de los efectos perjudiciales de los niveles aumentados de dióxido de carbono en el organismo humano. La investigadora pone de relieve que el CO2 también actúa mediante mecanismos no redox.
Puede leerse el artículo intitulado Production of Peroxymonocarbonate by Steady-State Micromolar H₂O₂ and Activated Macrophages in the Presence of CO2/HCO3– Evidenced by Boronate Probes en el siguiente enlace: https://pubs.acs.org/doi/10.1021/acs.chemrestox.4c00059.
*Con información del Redoxoma.
Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





