


En la imagen de la izquierda es posible observar a la enzima RdRp del SARS-CoV-2 (en rojo), que regula la replicación viral, en el interior del linfocito T CD4. En tanto, en la imagen de la derecha, las manchas verdes corresponden a las proteínas de la espícula del SARS-CoV-2 (spike proteins) situadas cerca de la membrana de la célula de defensa humana (imagen: Henrique Marques-Souza/Unicamp)
Experimentos realizados por científicos brasileños con linfocitos aislados en pacientes con COVID-19 indican que el virus se vale de la proteína CD4 para invadir un tipo de células clave en la coordinación de la respuesta antiviral
Experimentos realizados por científicos brasileños con linfocitos aislados en pacientes con COVID-19 indican que el virus se vale de la proteína CD4 para invadir un tipo de células clave en la coordinación de la respuesta antiviral
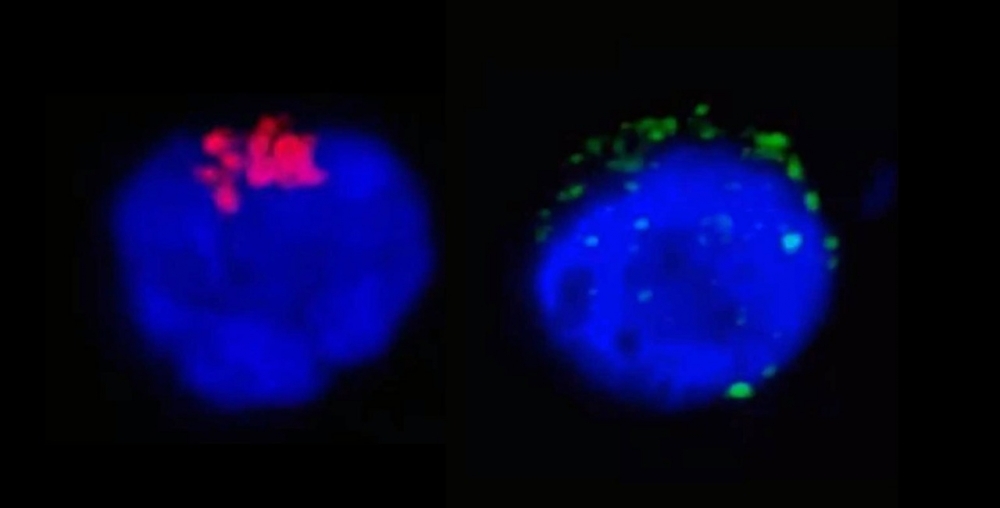
En la imagen de la izquierda es posible observar a la enzima RdRp del SARS-CoV-2 (en rojo), que regula la replicación viral, en el interior del linfocito T CD4. En tanto, en la imagen de la derecha, las manchas verdes corresponden a las proteínas de la espícula del SARS-CoV-2 (spike proteins) situadas cerca de la membrana de la célula de defensa humana (imagen: Henrique Marques-Souza/Unicamp)
Por Karina Toledo | Agência FAPESP – Un estudio coordinado por científicos de la Unicamp, la Universidad de Campinas (en el estado de São Paulo, Brasil) y dado a conocer en la plataforma medRxiv aporta nuevas evidencias que indican que el virus SARS-CoV-2 tiene la capacidad de infectar y de replicarse en el interior de linfocitos: puede provocar la muerte de las células de defensa y comprometer al menos temporalmente la acción del sistema inmunológico.
Según los autores, el nuevo coronavirus opera mediante un mecanismo análogo al del VIH, causante del sida. Ambos afectan a un tipo de linfocitos conocidos como T CD4, que se encargan de coordinar la llamada respuesta inmune adaptativa, ayudando tanto a los linfocitos B a producir anticuerpos como a los linfocitos T CD8 (encargados de reconocer y matar a las células infectadas) a proliferar. Esta coordinación transcurre mediante la liberación de moléculas de señalización conocidas como citoquinas.
“Nuestros resultados sugieren que, en algunos pacientes, el nuevo coronavirus puede provocar un cuadro de inmunodeficiencia aguda no solamente porque mata a una parte de los linfocitos T CD4, sino también porque perjudica la función de esas células. Esto lleva a que los linfocitos T CD8 proliferen menos y los linfocitos B produzcan anticuerpos con menor afinidad y duración. Sería un efecto similar al del VIH, pero agudo”, le explica a Agência FAPESP Alessandro Farias, jefe del Departamento de Genética, Evolución, Microbiología e Inmunología del Instituto de Biología (IB) de la Unicamp, quien coordinó la investigación junto al profesor Marcelo Mori.
Las conclusiones de este artículo, aún en proceso de revisión por pares, se basan fundamentalmente en experimentos con cultivos primarios de linfocitos (aislados en la sangre de voluntarios no infectados y de pacientes con COVID-19) realizados en el Laboratorio de Estudios de Virus Emergentes (Leve) del IB-Unicamp, con el apoyo de la FAPESP.
Durante la primera etapa del estudio, los investigadores incubaron células de donantes sanos con el SARS-CoV-2 y realizaron un seguimiento de lo que sucedía en las 24 horas siguientes mediante diferentes técnicas, tales como la de hibridación in situ, la microscopía electrónica de transmisión y la RT-PCR (la misma aplicada para diagnosticar la infección en la fase aguda).
“Realizamos este ensayo únicamente con linfocitos T CD4 y T CD8 porque son los tipos que aparecen más en merma en los pacientes con COVID-19 grave. Los análisis confirmaron la presencia del nuevo coronavirus en el interior de aproximadamente el 40% de los T CD4, y el 10% de esas células murieron al final del período de observación. Los linfocitos T CD8 no fueron afectados”, comenta Farias.
Los investigadores observaron también que la carga viral se duplicó con creces entre las mediciones realizadas dos y 24 horas después del comienzo de la prueba, una señal de que el virus estaba replicándose en las células del cultivo.
El paso siguiente consistió en analizar con las mismas herramientas los linfocitos T CD4 aislados en pacientes diagnosticados con COVID-19, en busca de señales del SARS-CoV-2. En las personas que padecían cuadros moderados de la enfermedad se hallaron pocos linfocitos infectados, y estaban produciendo, tal como era de esperarse, la citoquina interferón gamma (IFN-γ), importante para la respuesta antiviral. En tanto, en los pacientes graves, aparte de que existía una cantidad mucho mayor de linfocitos con el virus, esas células estaban produciendo interleuquina-10 (IL-10), una citoquina con acción antiinflamatoria, en lugar de la IFN-γ. Es decir que, en esos enfermos con COVID-19 severo, los linfocitos T CD4 estaban señalizándole al sistema inmunológico la necesidad de detener el combate contra el virus.
Según Farias, esto explicaría por qué en muchas personas que están en esas condiciones se registran alteraciones en la respuesta inmune adaptativa (que es específica para cada patógeno), tales como linfopenia (la merma de la concentración general de linfocitos en la sangre), agotamiento de linfocitos T y producción comprometida de anticuerpos.
“La producción de IL-10 desconecta el sistema inmunológico y le permite al virus permanecer durante más tiempo en el organismo. Por ahora sigue siendo imposible saber cuál es la causa de ello y cuáles son las consecuencias, es decir, si esos pacientes evolucionaron hacia la forma grave porque tenían más linfocitos T CD4 infectados o lo contrario. Pero existe una clara asociación entre esos dos factores”, afirma Farias.
Para abrir paso
Diversos estudios ya publicados apuntan que la molécula ACE-2 (enzima convertidora de angiotensina 2, por sus siglas en inglés) constituye la principal puerta de entrada del SARS-CoV-2 en la superficie de las células humanas. Sin embargo, se sabe que los linfocitos T CD4 expresan una cantidad muy pequeña de esta enzima sobre la superficie de su membrana plasmática, que está recubierta por la proteína que les da su nombre a estas células: CD4.
Para develar la estrategia que utiliza el nuevo coronavirus a los efectos de entrar en esos linfocitos –que normalmente son refractarios a la infección por virus y bacterias– el grupo de la Unicamp realizó dos nuevos test con las muestras de donantes sanos. En el primero, antes de insertar el virus, se dispusieron en el cultivo celular anticuerpos capaces de neutralizar a la proteína CD4. Y en el segundo experimento, se colocaron anticuerpos contra la ACE-2.
“Nuestra hipótesis indicaba que el SARS-CoV-2 lograría ingresar a la célula valiéndose únicamente de CD4, pero cuando neutralizamos también a la proteína ACE-2, se bloqueó totalmente la infección. Esto demuestra que, aun en pequeñas cantidades, la proteína ACE-2 es necesaria para que se concrete la invasión de los linfocitos”, dice Farias.
Ensayos de interacción entre moléculas in vitro revelaron que la proteína de la espícula del SARS-CoV-2, aquella que forma la corona presente en la superficie viral, es capaz de unirse a las proteínas CD4 de los linfocitos.
“Creemos que el virus se vale de una artimaña para ingresar en esas células. Utiliza la proteína CD4 únicamente para ubicarse cerca de la membrana celular y así localizar a la proteína ACE-2, que entonces le permite el paso hacia el medio intracelular”, explica el investigador.
Durante la tercera y última etapa de la investigación, realizada en colaboración con el profesor de la Universidad de São Paulo (USP) Helder Nakaya, los científicos aplicaron técnicas de bioinformática para reanalizar datos de un estudio publicado por investigadores chinos en mayo en la revista Nature Medicine, en el cual se concretó la secuenciación de leucocitos aislados en las secreciones pulmonares de pacientes con COVID-19 grave mediante una técnica conocida como single-cell sequencing.
“El algoritmo desarrollado por el grupo de Nakaya permitió identificar el genoma viral también en los linfocitos que estaban en los pulmones de los pacientes, lo cual aporta un nuevo nivel de evidencia y una mayor confiabilidad a los hallazgos”, afirma Farias.
La investigación contó también con la colaboración de investigadores de la Universidade Estadual Paulista (Unesp), del Centro Nacional de Investigaciones en Energía y Materiales (CNPEM), de la Fundación Oswaldo Cruz (Fiocruz) y del Instituto D’Or de Pesquisa e Ensino (Idor). El apoyo de la FAPESP se concretó mediante diversas ayudas y becas, a saber: 19/16116-4, 19/06372-3, 20/04583-4, 13/08293-7, 20/04579-7, 15/15626-8, 18/14933-2, 20/04746-0, 19/00098-7, 20/04919-2, 17/01184-9, 19/17007-4, 19/22398-2, 19/05155-9, 19/06459-1, 19/04726-2, 17/23920-9, 16/24163-4 y 16/23328-0.
En este momento, el grupo procura detallar más minuciosamente los efectos causados por la entrada del SARS-CoV-2 en los linfocitos T CD4. El objetivo es hallar formas de intervenir en este proceso, lo cual teóricamente podría ayudar a combatir la infección.
“Ya tenemos linfocitos aislados en más de 350 pacientes que pretendemos utilizar en los experimentos de laboratorio, y también realizaremos pruebas con ratones genéticamente modificados para expresar la ACE-2 humana. Una de las ideas consiste en evaluar el efecto de moléculas capaces de inhibir la interacción entre la proteína de la espícula del virus y la proteína CD4”, adelanta el investigador.
Puede leerse el artículo intitulado SARS-CoV-2 Uses CD4 to Infect T Helper Lymphocytes en el siguiente enlace: www.medrxiv.org/content/10.1101/2020.09.25.20200329v1.full.pdf.


Republicar
The Agency FAPESP licenses news via Creative Commons (CC-BY-NC-ND) so that they can be republished free of charge and in a simple way by other digital or printed vehicles. Agência FAPESP must be credited as the source of the content being republished and the name of the reporter (if any) must be attributed. Using the HMTL button below allows compliance with these rules, detailed in Digital Republishing Policy FAPESP.





