Registro de produtos para controle biológico de pragas ultrapassa o de agroquímicos no Brasil
Cerca de 90% da área voltada ao cultivo de cana-de-açúcar no país hoje já utiliza inimigos naturais para o combate de pragas agrícolas; dados foram apresentados durante a FAPESP Week Illinois
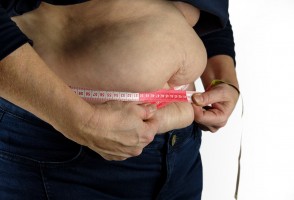
Obesidade abdominal associada à fraqueza muscular é condição que mais eleva risco de síndrome metabólica
Estudo feito por pesquisadores da UFSCar e da University College London acompanhou por oito anos quase 4 mil pessoas com mais de 50 anos
Grupo internacional faz simulações capazes de descrever com precisão inédita o clima na América do Sul
Objetivo é criar modelo de visualização computacional que represente com maior acurácia os processos hidroclimáticos que ocorrem na região e subsidiar medidas de adaptação às mudanças climáticas; iniciativa foi apresentada durante a FAPESP Week Illinois

Em palestra a empresários, ganhadores do Prêmio Nobel destacam a importância da pesquisa básica
Evento, realizado na sede da Federação das Indústrias do Estado de São Paulo, foi o terceiro e último da série “Criando o nosso futuro juntos com a ciência”, que trouxe ao Brasil os pesquisadores Serge Haroche, May-Britt Moser e David MacMillan
FAPESP recebe propostas para novas Escolas de Ciência Avançada até 3 de maio
Os cursos apoiados no âmbito da modalidade ESPCA devem promover discussões nas fronteiras da pesquisa em qualquer área do conhecimento
USP apresenta sete novos centros de estudos ligados diretamente à reitoria
Temas fundamentais da atualidade, como inteligência artificial, mudanças climáticas, câncer e instituições brasileiras, serão foco de ensino e pesquisa interinstitucional e multidisciplinar; nova organização confere mais autonomia e agilidade aos grupos
Cientistas transformam casca de banana em bioplástico para embalar alimentos
Material desenvolvido por grupos da Embrapa Instrumentação e da UFSCar tem propriedades antioxidantes, oferece proteção contra a radiação ultravioleta e não gera resíduos
OPORTUNIDADES FAPESP
PD em modelagem de cenários
SemeAr/Embrapa Agricultura Digital
Inscrições até 25/04/2024
PD em astrofísica de partículas
IFGW-Unicamp
Inscrições até 25/04/2024
TT-4 em sensoriamento remoto
Inpe
Inscrições até 24/04/2024
PD em informática em saúde pública
FMRP-USP
Inscrições até 22/04/2024
PD em física experimental com átomos frios, biofotônica e nanoplasmônica
CEPOF/IFSC-USP
Inscrições até 22/04/2024
Em palestra a empresários, ganhadores do Prêmio Nobel destacam a importância da pesquisa básica
FAPESP recebe propostas para novas Escolas de Ciência Avançada até 3 de maio
Obesidade abdominal associada à fraqueza muscular é condição que mais eleva risco de síndrome metabólica
USP apresenta sete novos centros de estudos ligados diretamente à reitoria
Cientistas transformam casca de banana em bioplástico para embalar alimentos
FAPESP e agência britânica vão apoiar projetos em ciências ambientais
Grupo internacional faz simulações capazes de descrever com precisão inédita o clima na América do Sul
Consórcio que inclui brasileiros sequencia o genoma referência do café arábica
FAPESP anuncia supervisores para chamada com Unesco/TWAS
Conferência Nacional de CT&I mobiliza debates em todo o país
Teorias que explicam crise na democracia não se adequam à América Latina, dizem especialistas
Tecnologias quânticas precisam atrair mais engenheiros
Capítulo 6: Viagem ao rio Negro marcou reencontro após expedições pioneiras nos anos 1990

Uma das artes de pesca utilizadas para coletar peixes-elétricos na Expedição DEGy Rio Negro foi empregada pela primeira vez em larga escala em água doce no projeto Calhamazon, que reuniu pesquisadores do Brasil e dos Estados Unidos entre 1993 e 1996
Capítulo 5: Acidente com raia não atrapalha o ritmo das coletas no Jauaperi

Baixa gravidade da lesão, atendimento médico rápido e cuidados adequados fizeram com que pesquisador pudesse voltar aos trabalhos no mesmo dia em que foi ferroado por peixe peçonhento. Na Amazônia, casos muitas vezes se agravam por carência de assistência especializada
Capítulo 4: Sarapós se destacam pela diversidade de ambientes que ocupam

Os mais abundantes peixes-elétricos estão presentes desde o fundo dos grandes rios até os igarapés, onde podem se enterrar na areia ou se confundir com o folhiço. Em duas semanas, expedição na bacia do rio Negro coletou 27 espécies do grupo
O Legado Suíço-Brasileiro na Amazônia: Arte, Ciência e Sustentabilidade
02/03/2024 a 30/04/2024
Física Moderna para a Sala de Aula
23/03/2024 a 20/04/2024
Introdução à programação com Python para alunas do ensino médio ou concluintes
30/03/2024 a 27/04/2024
Minicursos para estudantes do ensino médio 2024
06/04/2024 a 08/06/2024
Treinamento de plataformas e bases de dados científicas
09/04/2024 a 30/04/2024
14º Workshop Internacional sobre Interações Neutrino-Núcleo
15/04/2024 a 20/04/2024
Teste irá permitir detecção pouco invasiva de micrometástases
Startup desenvolve com apoio do PIPE-FAPESP solução que detecta biomolécula relacionada à presença de células migratórias de câncer bucal
Tecnologia pode possibilitar produção de enzimas no Brasil
Startup desenvolve tratamento alternativo para dermatite atópica
Teste irá permitir detecção pouco invasiva de micrometástases
Startup desenvolve com apoio do PIPE-FAPESP solução que detecta biomolécula relacionada à presença de células migratórias de câncer bucal
Chamadas FAPESP
Comunicar Ciência
Prazo: 22/01
Belmont Forum Climate, Environment, and Health
Prazo: Jan 2024
PIPE Start FAPESP-Sebrae: iniciando a jornada empreendedora de base tecnológica
Prazo: 18/03
Centros de Pesquisa em Inteligência Artificial Aplicada à Saúde
Prazo: 18/03
Fundação Nacional de Ciência da Suíça
Prazo: 22/03
Apoio a pesquisa em citricultura
Prazo: 31/03
Expedições Científicas Amazônia+10
Prazo: 29/04